

(圖片來源:Angew. Chem. Int. Ed.)
正文
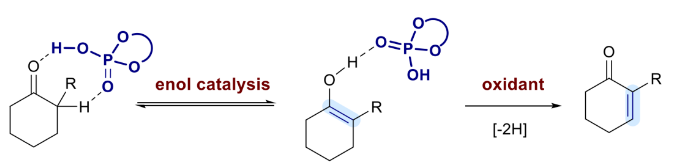
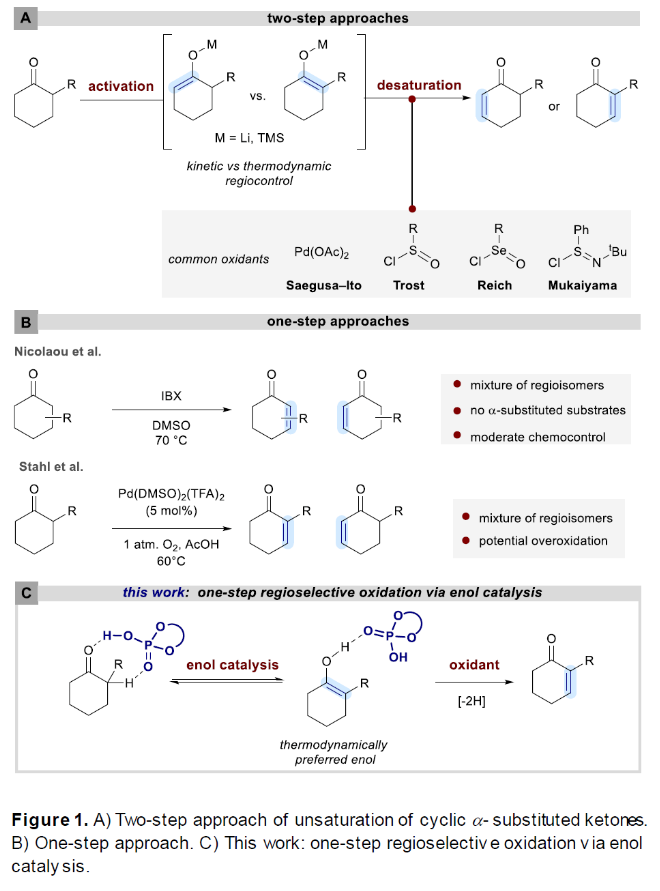
利用羰基化合物的脫氫反應轉化為相應的α,β-不飽和化合物是復雜分子和天然產物合成中經常遇到的轉化。常用的合成方法為利用酮轉化為烯醇或烯醇硅醚的活化策略,通過兩步來實現脫氫過程(Figure 1-A)。在反應中,熱力學或動力學控制的去質子化過程決定了后續氧化過程的區域選擇性。雖然Reich, Trost, Mukaiyama等課題組發展的硫化物氧化以及Saegusa–Ito所發展的化學計量鈀氧化過程可以實現此類轉化,但硫化物的高毒性以及鈀氧化劑的高成本限制了其應用。最近,Baran課題組發展的電化學方法以及Larock課題組報道的催化量Pd(OAc)2和氧氣結合實現的脫氫過程可以避免此類問題。隨后,Stahl課題組基于鈀氧化策略,發展了鈀催化非活化酮的直接氧化,一步實現了α,β-不飽和酮的制備(Figure 1-B)。此外,Nicolaou課題組還利用高價碘試劑直接實現了酮的一步脫氫反應。雖然上述一步反應策略展現了更為先進的去飽和方法,并且常用于全合成中,但其區域控制差和需要對易于氧化的官能團進行保護等不足限制了它們的普遍適用性。最近,德國馬克斯-普朗克研究所Benjamin List課題組利用DDQ作氧化劑,發展了BINOL衍生的磷酸催化α-取代環酮的高區域選擇性一步脫氫反應,為α-芳基和α-烷基取代的α,β-不飽和酮的合成提供了新的可靠途徑。(Figure 1-C)。下載化學加APP到你手機,更加方便,更多收獲。
(圖片來源:Angew. Chem. Int. Ed.)
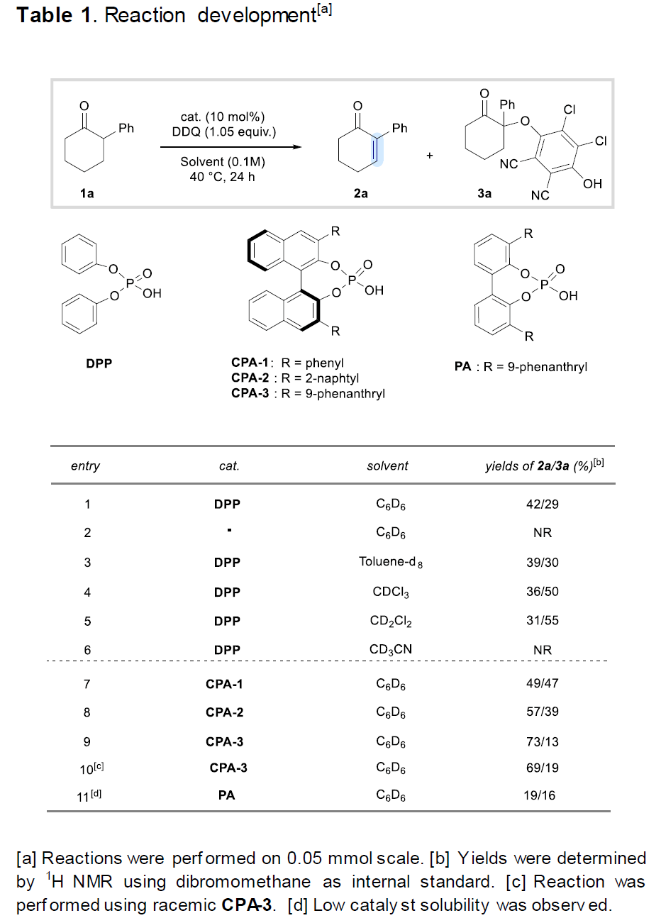
首先,作者選擇2-苯基環己酮1a作為模板底物進行反應探索(Table 1)。當使用BINOL衍生的磷酸催化劑CPA-3 (10 mol%), DDQ (1.05 equiv), 在苯 (0.1 M) 中40 °C反應24小時可以以73%的核磁產率,72%的分離產率得到產物2a(Table 1, entry 9)。此外,在反應過程中,作者還觀察到了α-醚化產物3a (13%)(DDQ加合物)。作者還嘗試將副產物3a原位轉化為所需的烯酮2a,但并未實現。
(圖片來源:Angew. Chem. Int. Ed.)
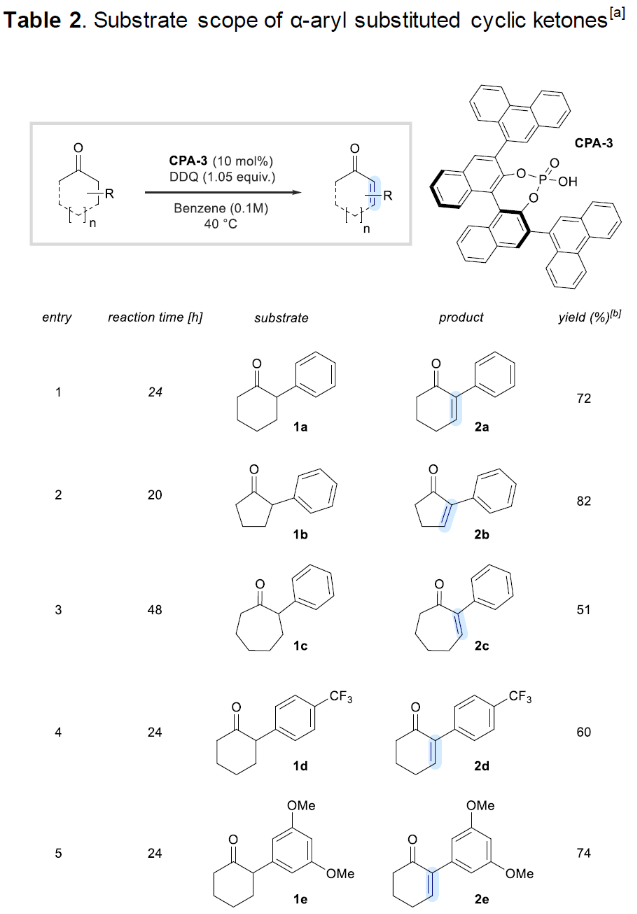
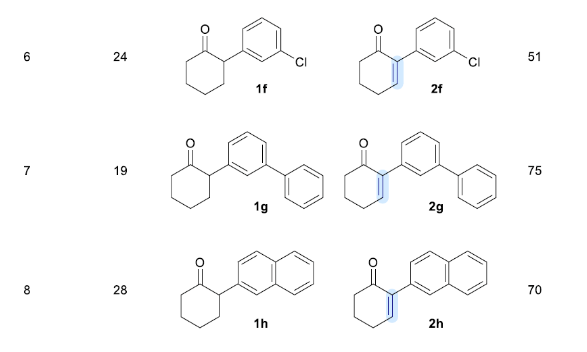
隨后,作者對此反應的底物范圍進行了考察。首先,作者對α-芳基取代的環酮進行了考察(Table 2)。實驗結果表明,α-苯基取代的環己酮、環戊酮以及環庚酮均可利用此轉化實現脫氫,分別以72%,82%和51%的產率得到相應的產物2a, 2b和2c。此外,不同電性和位阻取代基取代的α-苯基環己酮均可順利參與反應,以51-75%的產率得到相應的α,β-不飽和酮產物2d-2h。
(圖片來源:Angew. Chem. Int. Ed.)
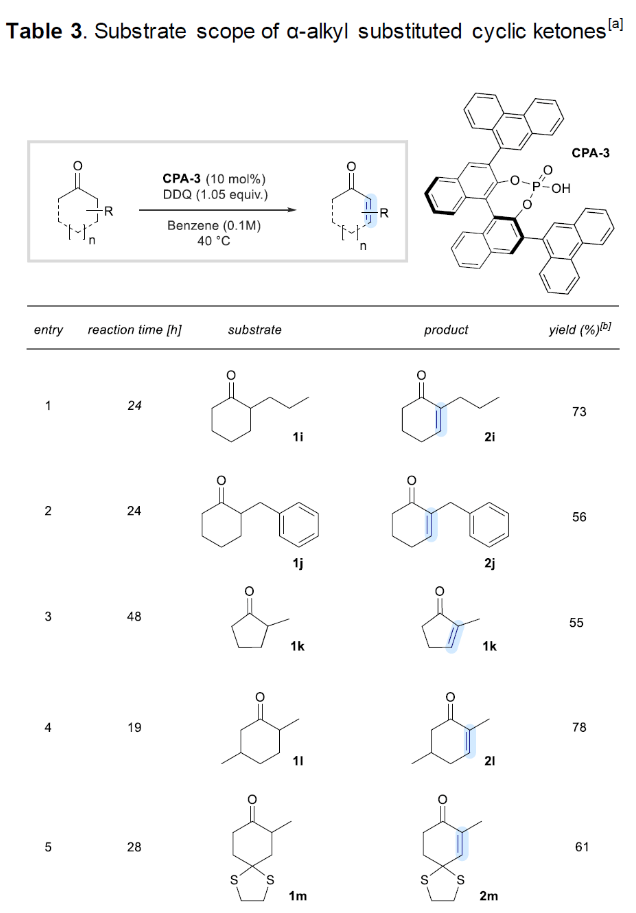
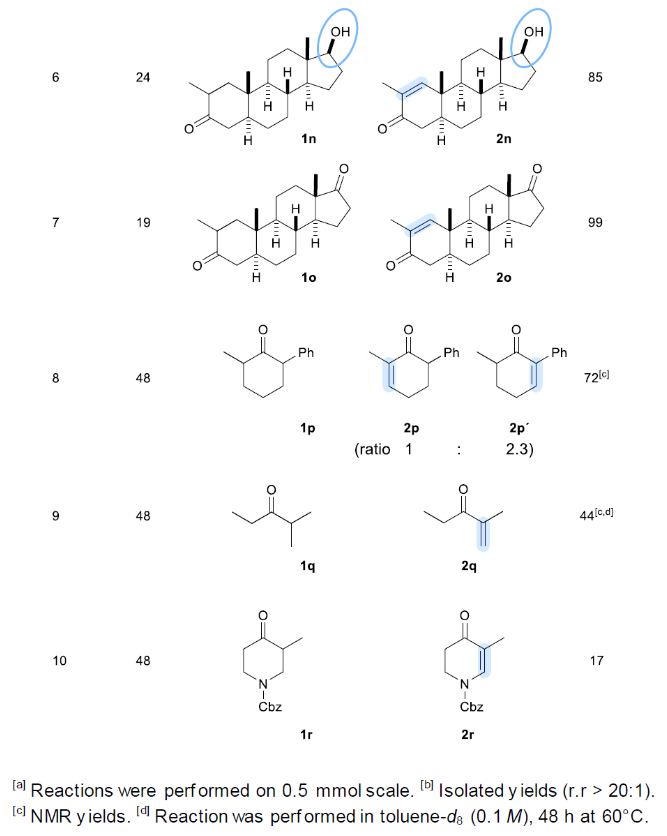
除此之外,作者對α-烷基取代的環酮進行了考察(Table 3)。實驗結果表明,對氧化條件敏感的基團如芐基、縮硫酮等均可兼容,分別以56%和61%的產率得到產物2j和2m。值得注意的是,α-烷基取代的甾體骨架也可順利參與轉化,以85%和99%的產率得到產物2n和2o,且分子內的羥基可以兼容且不被氧化(2n)。此外,Cbz保護的哌啶酮底物1r亦可兼容,以17%的產率得到產物2r。
(圖片來源:Angew. Chem. Int. Ed.)
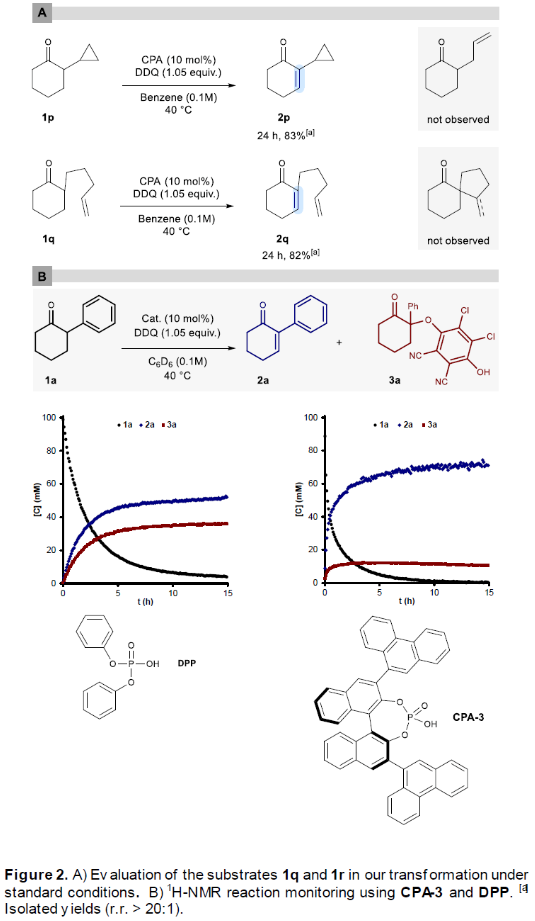
為了深入理解此轉化的反應機理,作者進行了控制實驗(Figure 2)。首先,自由基鐘實驗表明此轉化并不涉及自由基反應路徑(Figure 2-A)。隨后,作者利用核磁監測實驗得出DDQ加合物3a并不是此反應的中間體(Figure 2-B)。
(圖片來源:Angew. Chem. Int. Ed.)
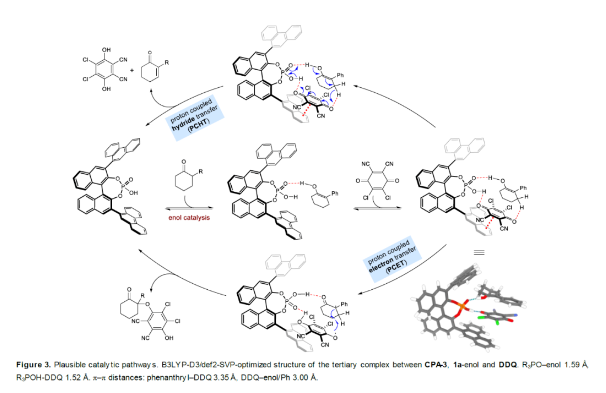
最后,作者提出了此轉化可能的反應機理(Figure 3)。首先,反應經歷類似于磷酸催化的Hantzsch酯轉移氫化反應機理來實現協同質子轉移。而鄰位的菲取代基可以通過與DDQ的π-π相互作用來穩定這種過渡態。兩種反應物由雙功能CPA催化劑通過兩個氫鍵緊密相連。整個絡合物形成一個三明治狀的結構,其通過與BINOL的3,3'-菲基以及富電子苯基取代的烯醇部分的π-π作用來穩定DDQ。此外,作者在B3LYP-D3/def 2-SVP水平上對CPA-3、烯醇1a和DDQ的絡合物進行了DFT計算,得到的理論結果與上述模型相一致。原位生成的烯醇與DDQ可能發生質子耦合電子轉移(PCET),并可以通過自由基再結合形成了醚化副產物。此外,作者還通過31P NMR表明,反應體系中磷酸會經歷緩慢衰變為未知的物種。
(圖片來源:Angew. Chem. Int. Ed.)
總結
德國馬克斯-普朗克研究所Benjamin List課題組發展了一步反應策略,高區域選擇性的實現了α-取代環酮的催化脫氫反應,且沒有過氧化副產物。此反應在BINOL衍生的磷酸催化劑CPA-3的催化下,高選擇性的得到了熱力學穩定的烯醇,并經歷隨后的DDQ氧化,以良好的產率,高選擇性的實現了一系列α,β-不飽和芳基或烷基取代烯酮產物的合成。此反應具有良好的底物適用性和官能團兼容性,為α,β-不飽和酮的合成提供了新的思路。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn