

(圖片來源:J. Am. Chem. Soc.)
烷基自由基與烯烴的分子間加成,即烯烴的氫-烷基化反應,在化學合成中被廣泛應用于碳-碳鍵的構建。最近,隨著溫和條件下促進的自由基反應的有效發展,如光氧化還原催化、電化學方法和地球含量豐富的過渡金屬催化,使得該化學的范圍和實用性進一步擴大,并為獲得對映體富集的手性結構砌塊和復雜分子的選擇性官能團化提供了新的催化策略。
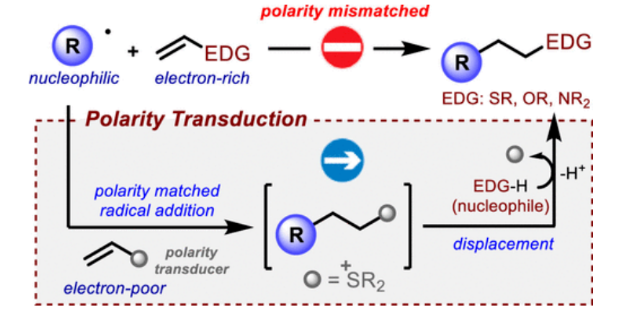
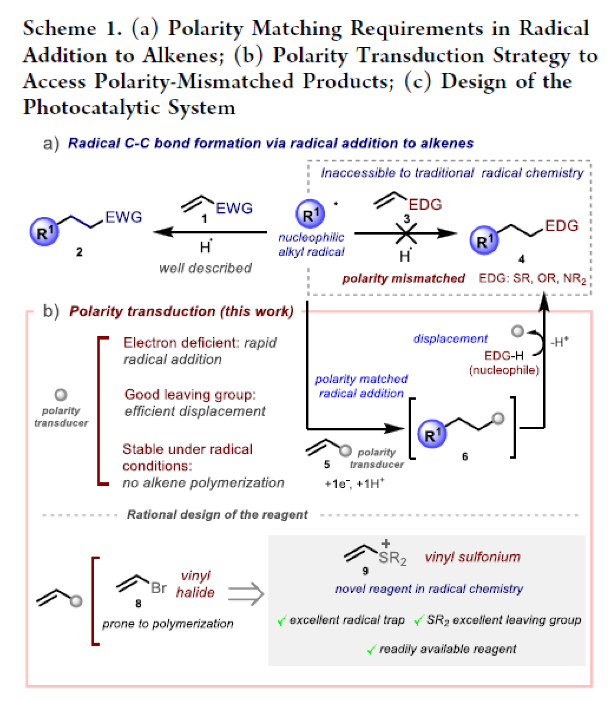
盡管這些過程具有一定的合成價值,但所涉及的自由基和烯烴之間嚴格的極性匹配要求是此化學發展的根本限制。雖然良好的前沿分子軌道相互作用確保了烷基自由基(通常親核)和缺電子烯烴1(Scheme 1a, left)之間的平穩反應,但利用相同的自由基與富電子烯烴3((Scheme 1a, right)反應在動力學上是不利的,且實際上是不會發生的,除非在自由基中心引入特定的缺電子官能團來誘導其親電特性。因此,使用傳統的自由基化學方法是不可能獲得產物4的。而在氫原子轉移過程的背景下,化學家們已經開發了一種策略來規避自由基化學中的不利極性要求—即極性反轉催化。然而,目前還沒有任何方法可以克服烯烴自由基加成的底物范圍限制。因此,發展解決上述底物范圍限制的通用方法將極大地改善自由基化學的應用領域,從而促進合成化學各個領域的進一步進展。最近,英國諾丁漢大學Mattia Silvi課題組發展了一種極性轉換策略,形式上克服了這種電性上的限制。乙烯基硫鎓離子被證明可以與碳中心自由基反應,使加合物可以進行原位或順序親核取代,從而獲得了利用傳統方法無法合成的產物。
作者認為由原位發生的兩個基本步驟相組合的設計思路將繞過上述限制,從而得到傳統方法難以合成的產物4。如Scheme 1b所示,在烯烴5上連接一個精心設計的官能團,其將起到類似于“極性傳感器”的作用。這個“極性傳感器”將發揮關鍵作用,將π體系中不匹配的富電子極性轉換為獲得產物4所需的匹配缺電子極性。隨后,在快速的自由基加成得到中間體6后,“極性傳感器”基團將被親核試劑取代,從而實現了產物4的合成。
在設計合適的“極性傳感器”官能團時,作者考慮了以下幾個方面的要求:1)其應該是缺電子性質的,從而降低相鄰π體系的電子密度,使得相應的LUMO軌道能量降低從而促進親核碳中心自由基的加成;2)其應該是一個好的離去基團,確保親核取代過程的快速發生;3)其結構和電子特征應該會抑制自由基聚合(這一過程通常在烯基鹵8中發生)。受到Barton課題組開創性的工作的啟發,作者認為乙烯基硫鎓離子9可以參與自由基共軛加成反應中,且硫鎓離子可以在分子間和分子內反應過程中作為好的離去基團。
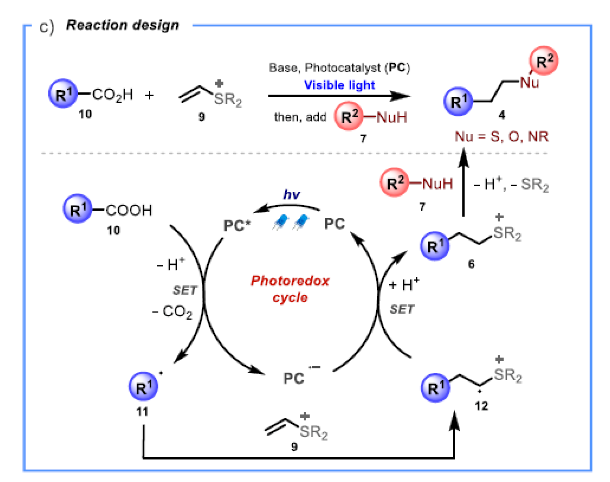
基于上述假設,作者設計了光催化反應。如Scheme 1c所示,羧酸10通過光催化劑誘導的單電子轉移脫羧氧化形成碳中心自由基11。由于缺電子硫鎓離子的誘導效應,親核自由基11將與9的端位烯基碳發生選擇性加成。接下來,缺電子自由基陽離子中間體12將與還原的光催化劑(PC??)經歷SET完成催化循環并得到瞬態的硫葉立德中間體并在反應條件下經歷質子化得到加合物6。最后,在體系中加入合適的親核試劑7發生親核取代從而得到目標產物4。
(圖片來源:J. Am. Chem. Soc.)
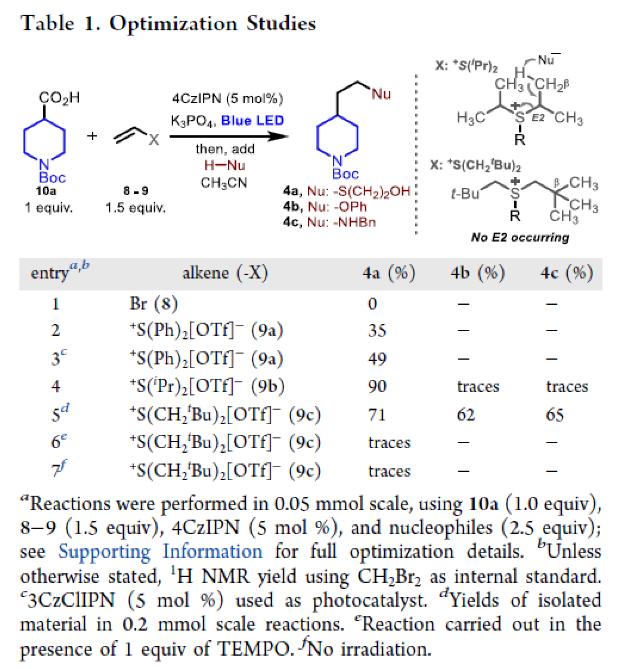
首先,作者選擇N-Boc異哌啶酸10a作為模板底物進行反應探索(Table 1)。通過一系列反條件篩選,作者發現當使用10a (1 equiv), 9c (1.5 equiv), 4CzIPN (5 mol %),在CH3CN中,藍光照射下室溫反應。隨后加入親核試劑 (2.5 equiv) 60 oC反應可以分別以71%、62%、65%的產率實現產物4a (Nu = S(CH2)2OH)、4b (Nu = OPh)、4c (Nu = NHBn)的合成(Table 1,entry 5)。控制實驗表明,在加入自由基捕獲劑TEMPO時(Table 1,entry 6)以及在不存在光照的條件下(Table 1,entry 7)反應均不發生。
(圖片來源:J. Am. Chem. Soc.)
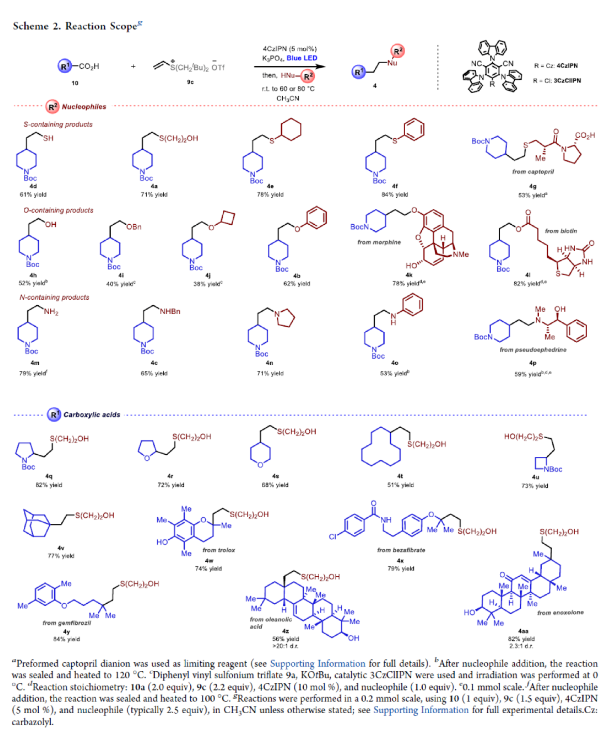
在得到了最優反應條件后,作者探索了此極性轉換策略的底物適用范圍(Scheme 2)。當使用一系列硫親核試劑,如硫氫化鈉(4d)、一級硫醇(4a, 4g)、二級硫醇(4e)、硫酚(4f),參與反應時,可以以良好的產率實現硫醇和硫醚產物的生成(53-84%)。此外,使用其它的氧親核試劑(4h-4l,38-82%)和氮親核試劑(4m-4p,53-79%)均可順利實現轉化,以中等至良好的產率得到了相應的加成產物。值得注意的是,一系列復雜的生物活性分子,如captopril(4g)、morphine(4k)、biotin(4l)、pseudoephedrine(4p)等均可與體系兼容。接下來,作者對一系列作為自由基前體的羧酸衍生物的兼容性進行了考察。實驗結果表明,一系列含氮、氧雜環的羧酸(4q-4s)、不同尺寸的環狀羧酸分子(4t-4v)均可參與反應。此外,一系列復雜生物活性分子衍生的羧酸,如Trolox(4w)、bezafibrate(4x)、gemfibrozil(4y)、oleanolic acid(4z)、enoxolone(4aa)等均可兼容,證明了此體系具有良好的普適性。
(圖片來源:J. Am. Chem. Soc.)
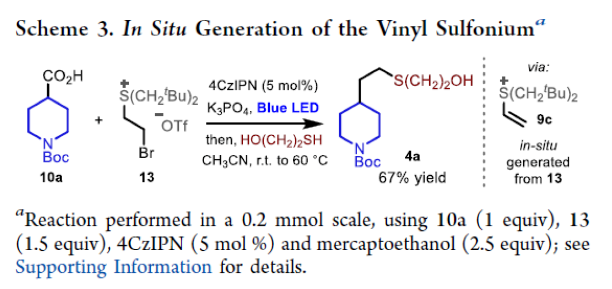
最后,作者利用13作為烯烴前體,在體系中原位生成烯烴9c后仍可以實現此轉化,以67%的產率實現產物4a的合成(Scheme 3)。
(圖片來源:J. Am. Chem. Soc.)
總結
英國諾丁漢大學Mattia Silvi課題組發展了一種極性轉換策略,形式上克服了自由基和烯烴加成過程中的嚴格極性匹配要求限制。利用碳中心自由基與乙烯基硫鎓離子加成,使加合物可以與不同的親核試劑進行原位或順序的親核取代,從而形式上獲得了利用傳統方法無法獲得的烷基自由基與富電子雙鍵的加成產物。該方法的發展重新定義了碳中心自由基與雙鍵加成的適用范圍。
文獻詳情:
Subhasis Paul, Dario Filippini, Mattia Silvi*, Polarity Transduction Enables the Formal Electronically Mismatched Radical Addition to Alkenes. J. Am. Chem. Soc. 2023
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn