- 首頁
- 資訊
Nat. Commun. :華中大羅亮團隊開發出可拉曼示蹤的活性氧響應型水凝膠用于腫瘤術后光動力-免疫聯合治療
來源:華中科技大學新聞網 2022-08-11
導讀:近日,華中科技大學生命科學與技術學院國家納米藥物工程技術研究中心羅亮教授團隊與中國藥科大學孫春萌教授合作開發出一種活性氧響應型水凝膠,用于免疫治療抗體在與光敏劑共存情況下的保護性遞送與持續釋放,并實現光動力治療與腫瘤免疫治療的長效協同。
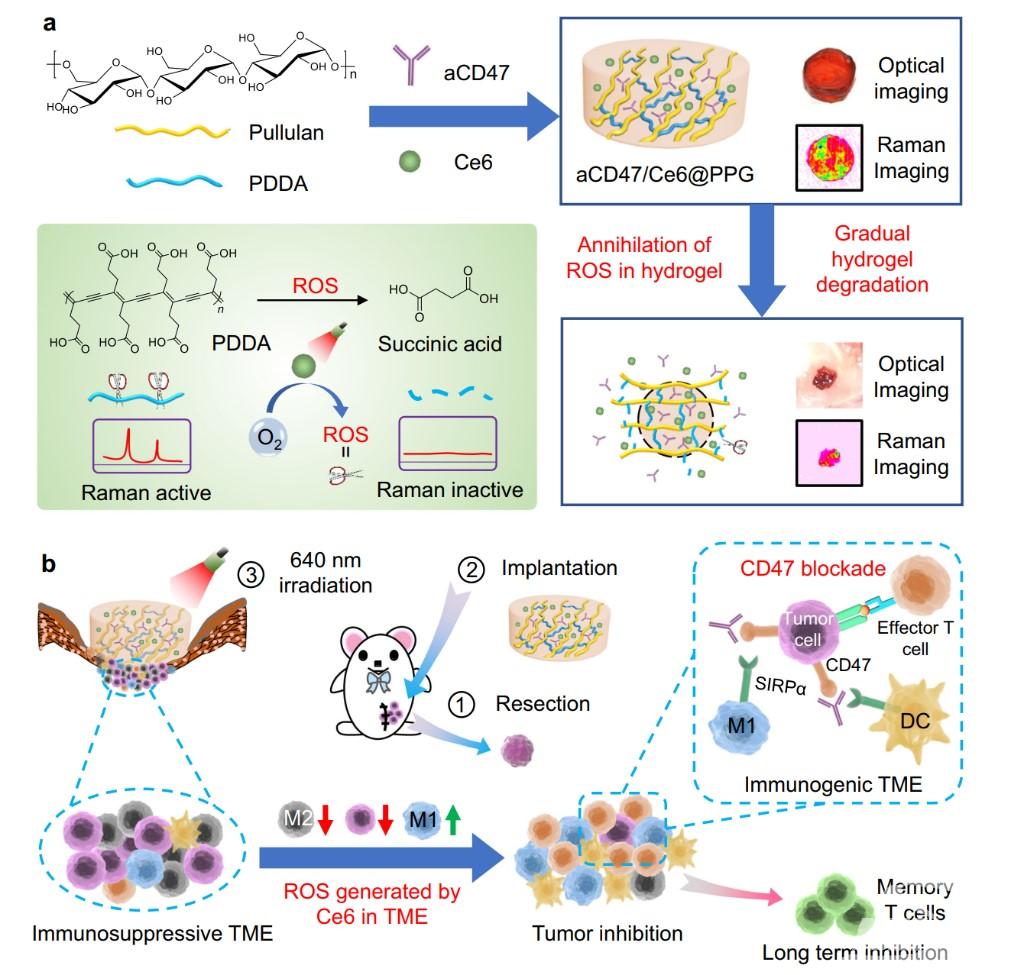
免疫檢查點阻斷(ICB)療法已成為多個腫瘤治療的一線療法,但其對免疫細胞浸潤不足的“冷腫瘤”療效有限的問題仍未得到有效解決。光動力療法(PDT)能夠誘導宿主免疫反應,與ICB聯合有望增強對“冷腫瘤”的免疫治療效果。然而,當光敏劑與免疫治療抗體共同遞送時,光敏劑在光照條件下產生的活性氧會不可避免地破壞抗體的活性,進而影響治療效果。
針對上述問題,華中科技大學生命科學與技術學院國家納米藥物工程技術研究中心羅亮教授團隊與中國藥科大學孫春萌教授合作開發出一種活性氧響應型水凝膠,用于免疫治療抗體在與光敏劑共存情況下的保護性遞送與持續釋放,并實現光動力治療與腫瘤免疫治療的長效協同。該工作以“Reactive oxygen species-responsive and Raman-traceable hydrogel combining photodynamic and immune therapy for postsurgical cancer treatment”為題,8月5日發表于《自然-通訊》。
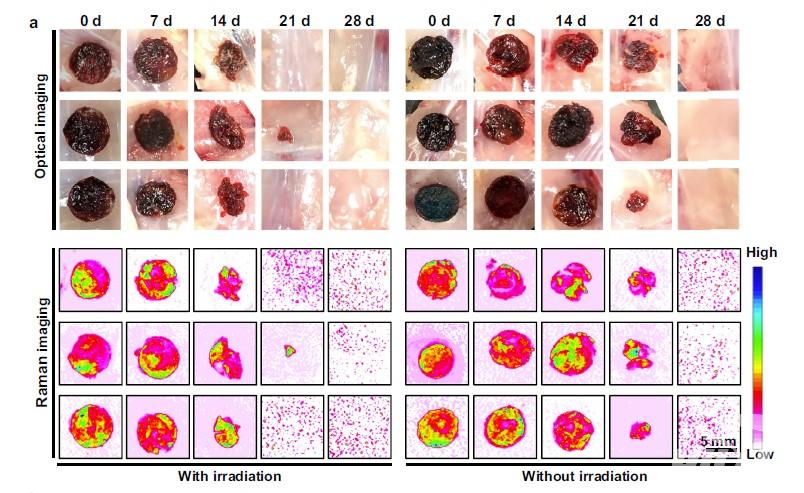
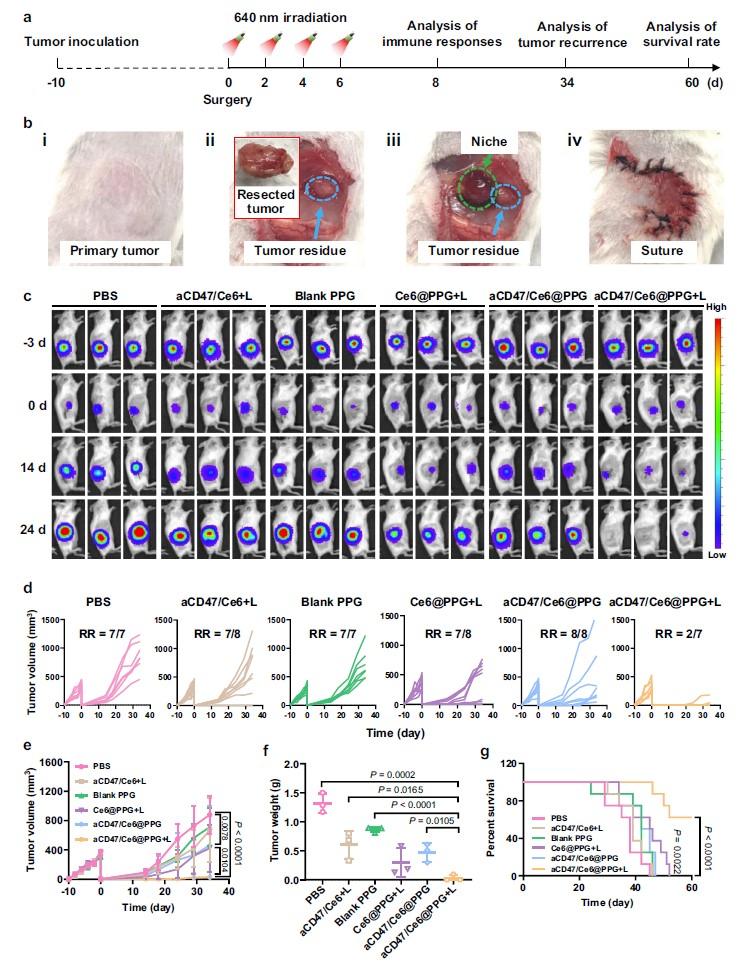
羅亮教授團隊前期報道了一種可在活性氧作用下完全降解的共軛高分子聚二炔衍生物PDDA(J. Am. Chem. Soc. 2021, 10054),其降解產物主要為生物相容性極佳的丁二酸。在此工作基礎上,該團隊進一步將PDDA與普魯蘭糖交聯制備得到一種活性氧響應型凝膠,并負載光敏劑Ce6與ICB抗體aCD47。在PDT的過程中,負載于凝膠內的Ce6所產生的活性氧易與共載的抗體反應,破壞抗體結構,降低抗體活性。此時,作為凝膠骨架之一的PDDA能夠有效清除凝膠內的ROS從而保護aCD47的活性;而且PDDA能夠在清除活性氧的同時發生降解,進而觸發凝膠降解,實現光敏劑和抗體的可控精準釋放。此外,該團隊前期工作還表明,PDDA在“細胞拉曼沉默區”(1800-2800cm-1)具有超強的拉曼信號,其單位強度可達一般小分子探針的105倍以上(Nat. Commun. 2020, 81;NanoLett.2022, 4544)。同時,PDDA的拉曼信號強度與其降解程度正相關,因此,可通過拉曼成像監控該活性氧響應型凝膠的體內降解與ROS的消耗情況。研究人員進一步將此活性氧響應型水凝膠應用于典型的“冷腫瘤”4T1腫瘤的術后模型。腫瘤切除后如何防止復發與轉移一直是臨床難點問題,而本實驗結果與預期一致,該載藥凝膠可以有效重塑腫瘤術后的免疫抑制微環境,并實現PDT與ICB的高效持續協同治療。采用PPG凝膠體系不僅能夠長期防止腫瘤切除后的復發與轉移,并且對于“再挑戰”模型也有良好的抑制效果。因此,基于可降解聚二炔衍生物PDDA的活性氧響應型水凝膠為PDT與ICB療法聯合使用提供了新思路。華中科技大學生命科學與技術學院為該論文第一單位,華中科技大學生命科學與技術學院碩士生張一漪、博士后田斯丹和黃麗萍、中國藥科大學博士生李亞楠為論文共同第一作者,羅亮教授為論文通訊作者。該研究得到中國藥科大學孫春萌教授和涂家生教授的大力支持和幫助,華中科技大學生命學院楊祥良教授、劉鋼教授和孟凡玲副教授也參與了該工作。此研究得到國家自然科學基金(21877042、22077038、22107032)、國家重點研發計劃(2018YFA0208903)、中國博士后科學基金(2017M622454、2020T130038ZX)和華中科技大學引進人才啟動經費的資助。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn