- 首頁(yè)
- 資訊
不僅限“助攻”病毒感染│陶亮課題組發(fā)現(xiàn)TMPRSS2還能介導(dǎo)索氏梭菌出血毒素的宿主入侵
來(lái)源:西湖大學(xué) 2022-07-28
導(dǎo)讀:近日,西湖大學(xué)生命科學(xué)學(xué)院的陶亮課題組在細(xì)菌毒素對(duì)宿主細(xì)胞功能的影響和作用機(jī)制的研究,先后發(fā)現(xiàn)了毒素TcdA, Tcnα, TcdB等的多個(gè)宿主細(xì)胞受體領(lǐng)域再次取得新的突破。北京時(shí)間2022年7月26日,團(tuán)隊(duì)在Nature Communications上在線發(fā)表題為“Paeniclostridium sordellii?hemorrhagic toxin targets TMPRSS2 to induce colonic epithelial lesions”的研究論文,首次揭示TMPRSS2是TcsH的腸上皮受體,填補(bǔ)了多年以來(lái)對(duì)出血毒素TcsH知之甚少的領(lǐng)域空白。
索氏梭菌(Paeniclostridium?sordellii)是一種產(chǎn)芽孢的革蘭氏陽(yáng)性細(xì)菌,可感染人和其他動(dòng)物引起組織壞死,腸毒血癥,敗血癥及中毒性休克等嚴(yán)重疾病。該細(xì)菌常見(jiàn)于環(huán)境中,并有一定幾率定植在人體腸道和女性生殖道中(約3-4%)。目前,索氏梭菌引發(fā)的急性感染病例總數(shù)不多但卻非常致命。約74%的索氏梭菌急性感染發(fā)生在女性分娩或流產(chǎn)過(guò)程,致死率接近100%。
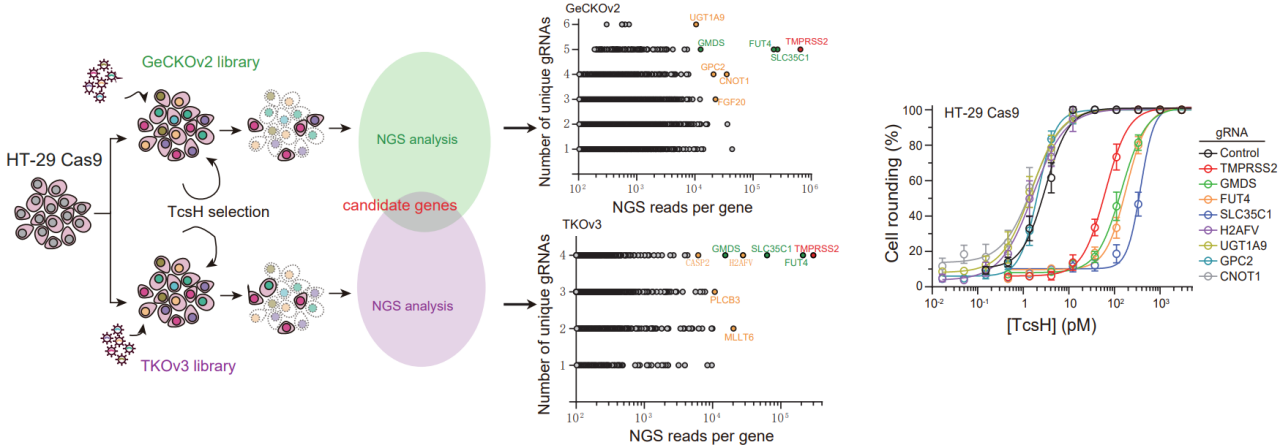
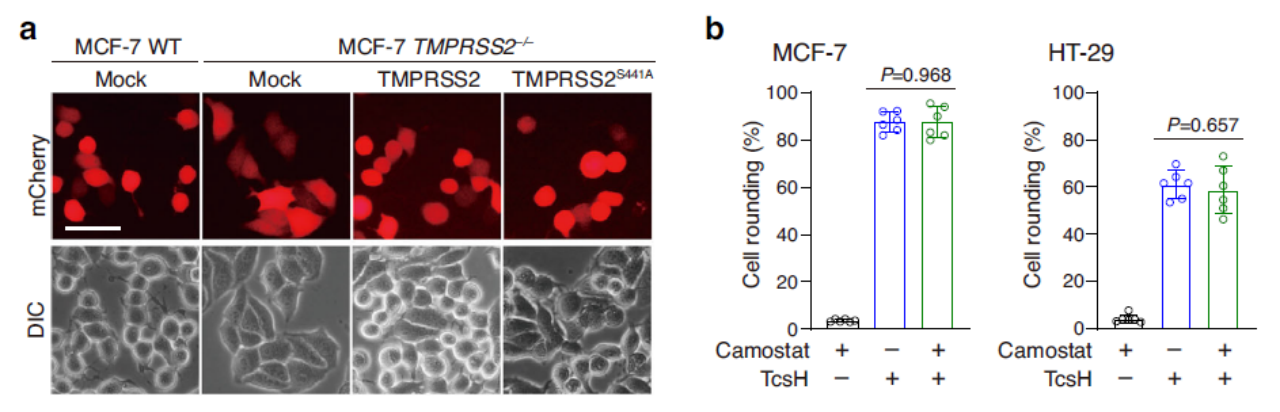
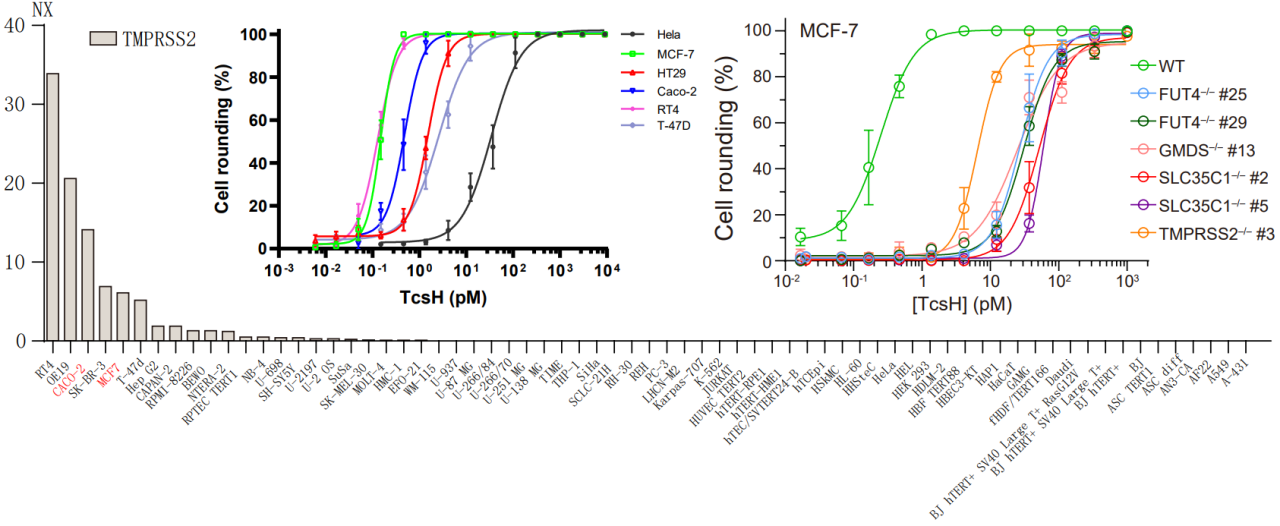
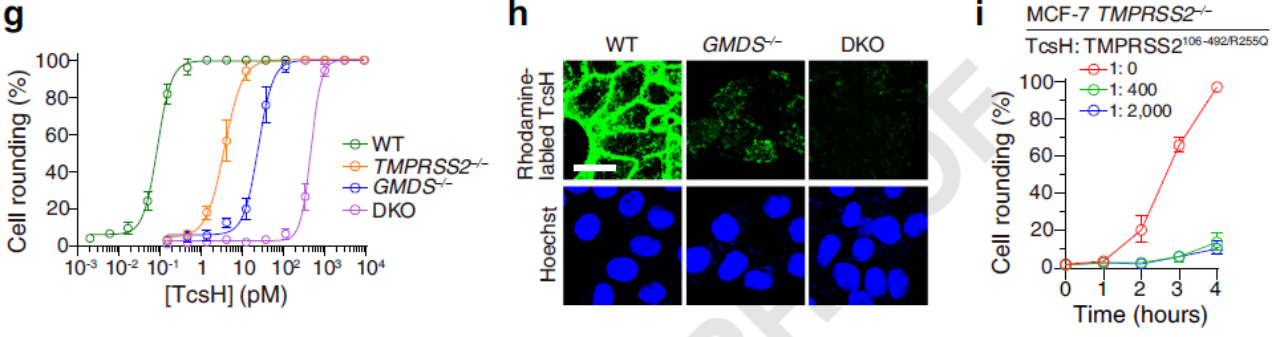
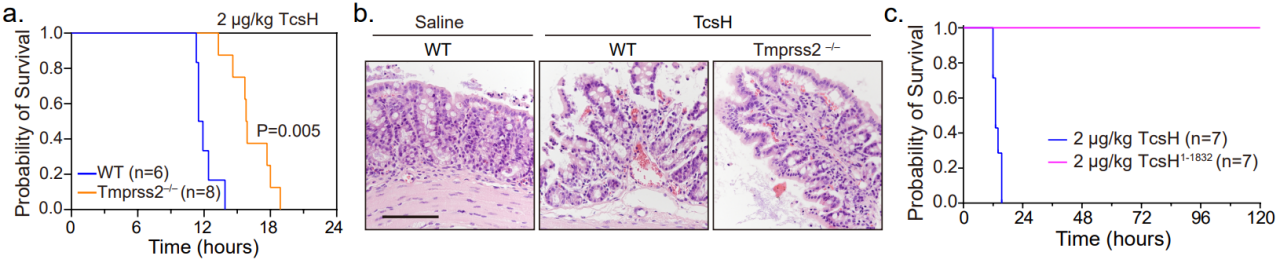
索氏梭菌毒力因子主要包括致死毒素TcsL和出血毒素TcsH,這兩種毒素均屬于大梭菌毒素(Large Clostridial Toxin, LCT)家族,該家族其他成員還包括艱難梭菌產(chǎn)生的毒素TcdA和TcdB,產(chǎn)氣莢膜梭菌的毒素TpeL以及諾維氏梭菌的毒素Tcnα等。TcsH是該毒素家族中唯一細(xì)胞受體尚未闡明的重要成員,這在很大程度上阻礙了我們對(duì)其作用機(jī)理和發(fā)病機(jī)制的研究。西湖大學(xué)生命科學(xué)學(xué)院的陶亮課題組專注于細(xì)菌毒素對(duì)宿主細(xì)胞功能的影響和作用機(jī)制的研究,先后發(fā)現(xiàn)了毒素TcdA, Tcnα, TcdB等的多個(gè)宿主細(xì)胞受體,部分研究成果已發(fā)表在Cell, Cell Research, Nature Microbiology等期刊上。近日,陶亮課題組在該領(lǐng)域再次取得新的突破。北京時(shí)間2022年7月26日,團(tuán)隊(duì)在Nature Communications上在線發(fā)表題為“Paeniclostridium sordellii?hemorrhagic toxin targets TMPRSS2 to induce colonic epithelial lesions”的研究論文,首次揭示TMPRSS2是TcsH的腸上皮受體,填補(bǔ)了多年以來(lái)對(duì)出血毒素TcsH知之甚少的領(lǐng)域空白。 由于可參考的關(guān)于TcsH的先前研究相對(duì)稀少,團(tuán)隊(duì)在初期也遇到了不小的困難。其中一個(gè)難點(diǎn)就是合適的與毒素互作的靶向細(xì)胞的選擇。與其它LCT相比,TcsH在很多常見(jiàn)細(xì)胞株上表現(xiàn)出來(lái)得毒性很弱。研究團(tuán)隊(duì)意識(shí)到篩選合適細(xì)胞系的重要性,于是測(cè)試了大量的不同組織來(lái)源的細(xì)胞系,多數(shù)人源細(xì)胞系對(duì)TcsH都不敏感,但研究中也發(fā)現(xiàn)了兩株特定的細(xì)胞,人結(jié)腸癌細(xì)胞系HT-29和人結(jié)直腸癌細(xì)胞系Caco-2,對(duì)TcsH高度敏感。基于這一發(fā)現(xiàn),團(tuán)隊(duì)選取了HT-29細(xì)胞作為研究TcsH的模式細(xì)胞,并且為了提高成功率,選擇兩個(gè)不同來(lái)源的人源sgRNA文庫(kù)在HT-29細(xì)胞上構(gòu)建敲除文庫(kù)。通過(guò)TcsH壓力篩選,研究者們發(fā)現(xiàn)這兩個(gè)獨(dú)立的篩選系統(tǒng)同時(shí)富集了一系列共同的靶向基因,包括跨膜絲氨酸蛋白酶2(TMPRSS2)及巖藻糖基化修飾相關(guān)基因GMDS、SLC35C1、FUT4(圖1)。通過(guò)構(gòu)建基因突變和回補(bǔ)細(xì)胞,研究者們證明這些基因?qū)?/span>TcsH的細(xì)胞侵入起了重要作用。圖1. CRISPR/Cas9介導(dǎo)的全基因組敲除篩選發(fā)現(xiàn)與TcsH作用相關(guān)的宿主基因TMPRSS2由于廣泛參與了包括流感、SARS、MERS等在內(nèi)的多種病毒的細(xì)胞入侵而“臭名昭著”。TMPRSS2參與病毒入侵的方式是通過(guò)其絲氨酸蛋白酶活性激活病毒的刺突蛋白,從而促進(jìn)膜融合。有意思的是,TMPRSS2的絲氨酸蛋白酶活性與其介導(dǎo)TcsH入侵完全無(wú)關(guān)(圖2)。另一方面,TMPRSS2可以特異性地與TcsH進(jìn)行結(jié)合,親和力高達(dá)0.13 nM。說(shuō)明與“助攻”病毒感染的模式不同,TMPRSS2是作為直接的蛋白受體協(xié)助毒素TcsH入侵靶向細(xì)胞的。圖2.TMPRSS2的絲氨酸蛋白酶活性缺失不影響介導(dǎo)TcsH的入侵值得一提的是,TMPRSS2僅在少部分細(xì)胞上有較高水平表達(dá),且其在細(xì)胞中的表達(dá)量與該細(xì)胞對(duì)TcsH的敏感性吻合,這也解釋了為何前期研究發(fā)現(xiàn)只有少數(shù)細(xì)胞株對(duì)TcsH是敏感的(圖3)。圖3. TMPRSS2高表達(dá)的細(xì)胞展現(xiàn)出對(duì)TcsH的高敏感性另一方面,巖藻糖基化修飾廣泛存在于許多細(xì)胞表面,研究發(fā)現(xiàn)其與TcsH在細(xì)胞表面的結(jié)合密切相關(guān)。通過(guò)進(jìn)一步的生化和細(xì)胞學(xué)實(shí)驗(yàn),包括構(gòu)敲除后補(bǔ)回實(shí)驗(yàn)、體外結(jié)合、競(jìng)爭(zhēng)拮抗等,研究者們證明了TMPRSS2和巖藻糖化的作用是相互獨(dú)立的,兩者可競(jìng)爭(zhēng)性地參與TcsH的細(xì)胞識(shí)別(圖4).圖4. TMPRSS2和巖藻糖化多糖可作為T(mén)csH兩類相互獨(dú)立的受體。最后,為進(jìn)一步探究TMPRSS2在生理和病理學(xué)上的意義,研究者們利用了一種Tmprss2全敲除的小鼠模型。腹腔注射毒素后發(fā)現(xiàn),野生型(Tmprss2+/+)和雜合型(Tmprss2+/?)小鼠對(duì)TcsH的耐受性顯著低于純合型(Tmprss2?/?)小鼠。由于腸道是索氏梭菌定植的重要部位之一,且已知部分腸道上皮細(xì)胞有較高的TMPRSS2表達(dá)。后續(xù)研究者們利用野生型和Tmprss2敲除小鼠構(gòu)建腸道結(jié)扎模型,結(jié)果顯示TcsH處理后Tmprss2敲除小鼠結(jié)腸上皮損傷明顯小于野生型小鼠(圖5)。圖5.小鼠模型顯示TMPRSS2是TcsH重要的病理相關(guān)受體西湖大學(xué)生命科學(xué)學(xué)院的陶亮研究員為本文通訊作者;陶亮課題組的博士研究生李星星和賀柳晴為共同第一作者;其他合作作者包括西湖大學(xué)的李顏顏博士,博士后羅建華,博士研究生鄭洋鈴、周瑤、李丹陽(yáng),及科研助理張媛媛和潘振瑞;此外還感謝西湖大學(xué)生科院的章永登研究員在熒光顯微攝影方面提供的幫助。本課題受到國(guó)家自然科學(xué)基金、西湖實(shí)驗(yàn)室(生命科學(xué)和生物醫(yī)學(xué)浙江省實(shí)驗(yàn)室)及西湖教育基金會(huì)的資助;項(xiàng)目實(shí)施還得到了西湖大學(xué)生物醫(yī)學(xué)實(shí)驗(yàn)技術(shù)中心和實(shí)驗(yàn)動(dòng)物中心的支持和幫助。西湖大學(xué)微生物宿主交互實(shí)驗(yàn)室(實(shí)驗(yàn)室主頁(yè):https://tao.lab.westlake.edu.cn/)致力于研究微生物-宿主之間的相互作用方式和內(nèi)在規(guī)律,尤其是從分子、生化、細(xì)胞、生信、結(jié)構(gòu)等方面研究重要病原細(xì)菌及其致病因子對(duì)宿主的影響及作用機(jī)制。西湖大學(xué)生命科學(xué)學(xué)院研究員陶亮近年來(lái)以通訊作者在Cell、Cell Research、Nature Microbiology、Nature Communications、PLOS Pathogens等學(xué)科主流期刊上發(fā)表多篇學(xué)術(shù)論文。實(shí)驗(yàn)室招收博士研究生,且有多個(gè)博士后、科研助理崗位,方向包括且不限于分子微生物學(xué)、生物信息學(xué)和微生物組學(xué)、生物化學(xué)、免疫學(xué)、細(xì)胞生物學(xué)等,誠(chéng)邀各方青年才俊加入、攜手共同成長(zhǎng)!(聯(lián)系方式:taoliang@westlake.edu.cn)參考資料:https://sls.westlake.edu.cn/NEWS/202207/t20220727_21812.shtml
由于可參考的關(guān)于TcsH的先前研究相對(duì)稀少,團(tuán)隊(duì)在初期也遇到了不小的困難。其中一個(gè)難點(diǎn)就是合適的與毒素互作的靶向細(xì)胞的選擇。與其它LCT相比,TcsH在很多常見(jiàn)細(xì)胞株上表現(xiàn)出來(lái)得毒性很弱。研究團(tuán)隊(duì)意識(shí)到篩選合適細(xì)胞系的重要性,于是測(cè)試了大量的不同組織來(lái)源的細(xì)胞系,多數(shù)人源細(xì)胞系對(duì)TcsH都不敏感,但研究中也發(fā)現(xiàn)了兩株特定的細(xì)胞,人結(jié)腸癌細(xì)胞系HT-29和人結(jié)直腸癌細(xì)胞系Caco-2,對(duì)TcsH高度敏感。基于這一發(fā)現(xiàn),團(tuán)隊(duì)選取了HT-29細(xì)胞作為研究TcsH的模式細(xì)胞,并且為了提高成功率,選擇兩個(gè)不同來(lái)源的人源sgRNA文庫(kù)在HT-29細(xì)胞上構(gòu)建敲除文庫(kù)。通過(guò)TcsH壓力篩選,研究者們發(fā)現(xiàn)這兩個(gè)獨(dú)立的篩選系統(tǒng)同時(shí)富集了一系列共同的靶向基因,包括跨膜絲氨酸蛋白酶2(TMPRSS2)及巖藻糖基化修飾相關(guān)基因GMDS、SLC35C1、FUT4(圖1)。通過(guò)構(gòu)建基因突變和回補(bǔ)細(xì)胞,研究者們證明這些基因?qū)?/span>TcsH的細(xì)胞侵入起了重要作用。圖1. CRISPR/Cas9介導(dǎo)的全基因組敲除篩選發(fā)現(xiàn)與TcsH作用相關(guān)的宿主基因TMPRSS2由于廣泛參與了包括流感、SARS、MERS等在內(nèi)的多種病毒的細(xì)胞入侵而“臭名昭著”。TMPRSS2參與病毒入侵的方式是通過(guò)其絲氨酸蛋白酶活性激活病毒的刺突蛋白,從而促進(jìn)膜融合。有意思的是,TMPRSS2的絲氨酸蛋白酶活性與其介導(dǎo)TcsH入侵完全無(wú)關(guān)(圖2)。另一方面,TMPRSS2可以特異性地與TcsH進(jìn)行結(jié)合,親和力高達(dá)0.13 nM。說(shuō)明與“助攻”病毒感染的模式不同,TMPRSS2是作為直接的蛋白受體協(xié)助毒素TcsH入侵靶向細(xì)胞的。圖2.TMPRSS2的絲氨酸蛋白酶活性缺失不影響介導(dǎo)TcsH的入侵值得一提的是,TMPRSS2僅在少部分細(xì)胞上有較高水平表達(dá),且其在細(xì)胞中的表達(dá)量與該細(xì)胞對(duì)TcsH的敏感性吻合,這也解釋了為何前期研究發(fā)現(xiàn)只有少數(shù)細(xì)胞株對(duì)TcsH是敏感的(圖3)。圖3. TMPRSS2高表達(dá)的細(xì)胞展現(xiàn)出對(duì)TcsH的高敏感性另一方面,巖藻糖基化修飾廣泛存在于許多細(xì)胞表面,研究發(fā)現(xiàn)其與TcsH在細(xì)胞表面的結(jié)合密切相關(guān)。通過(guò)進(jìn)一步的生化和細(xì)胞學(xué)實(shí)驗(yàn),包括構(gòu)敲除后補(bǔ)回實(shí)驗(yàn)、體外結(jié)合、競(jìng)爭(zhēng)拮抗等,研究者們證明了TMPRSS2和巖藻糖化的作用是相互獨(dú)立的,兩者可競(jìng)爭(zhēng)性地參與TcsH的細(xì)胞識(shí)別(圖4).圖4. TMPRSS2和巖藻糖化多糖可作為T(mén)csH兩類相互獨(dú)立的受體。最后,為進(jìn)一步探究TMPRSS2在生理和病理學(xué)上的意義,研究者們利用了一種Tmprss2全敲除的小鼠模型。腹腔注射毒素后發(fā)現(xiàn),野生型(Tmprss2+/+)和雜合型(Tmprss2+/?)小鼠對(duì)TcsH的耐受性顯著低于純合型(Tmprss2?/?)小鼠。由于腸道是索氏梭菌定植的重要部位之一,且已知部分腸道上皮細(xì)胞有較高的TMPRSS2表達(dá)。后續(xù)研究者們利用野生型和Tmprss2敲除小鼠構(gòu)建腸道結(jié)扎模型,結(jié)果顯示TcsH處理后Tmprss2敲除小鼠結(jié)腸上皮損傷明顯小于野生型小鼠(圖5)。圖5.小鼠模型顯示TMPRSS2是TcsH重要的病理相關(guān)受體西湖大學(xué)生命科學(xué)學(xué)院的陶亮研究員為本文通訊作者;陶亮課題組的博士研究生李星星和賀柳晴為共同第一作者;其他合作作者包括西湖大學(xué)的李顏顏博士,博士后羅建華,博士研究生鄭洋鈴、周瑤、李丹陽(yáng),及科研助理張媛媛和潘振瑞;此外還感謝西湖大學(xué)生科院的章永登研究員在熒光顯微攝影方面提供的幫助。本課題受到國(guó)家自然科學(xué)基金、西湖實(shí)驗(yàn)室(生命科學(xué)和生物醫(yī)學(xué)浙江省實(shí)驗(yàn)室)及西湖教育基金會(huì)的資助;項(xiàng)目實(shí)施還得到了西湖大學(xué)生物醫(yī)學(xué)實(shí)驗(yàn)技術(shù)中心和實(shí)驗(yàn)動(dòng)物中心的支持和幫助。西湖大學(xué)微生物宿主交互實(shí)驗(yàn)室(實(shí)驗(yàn)室主頁(yè):https://tao.lab.westlake.edu.cn/)致力于研究微生物-宿主之間的相互作用方式和內(nèi)在規(guī)律,尤其是從分子、生化、細(xì)胞、生信、結(jié)構(gòu)等方面研究重要病原細(xì)菌及其致病因子對(duì)宿主的影響及作用機(jī)制。西湖大學(xué)生命科學(xué)學(xué)院研究員陶亮近年來(lái)以通訊作者在Cell、Cell Research、Nature Microbiology、Nature Communications、PLOS Pathogens等學(xué)科主流期刊上發(fā)表多篇學(xué)術(shù)論文。實(shí)驗(yàn)室招收博士研究生,且有多個(gè)博士后、科研助理崗位,方向包括且不限于分子微生物學(xué)、生物信息學(xué)和微生物組學(xué)、生物化學(xué)、免疫學(xué)、細(xì)胞生物學(xué)等,誠(chéng)邀各方青年才俊加入、攜手共同成長(zhǎng)!(聯(lián)系方式:taoliang@westlake.edu.cn)參考資料:https://sls.westlake.edu.cn/NEWS/202207/t20220727_21812.shtml
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來(lái)源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn