



(圖片來源: Nat. Commun.)
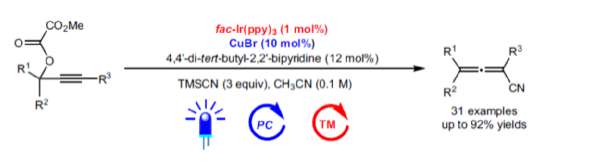
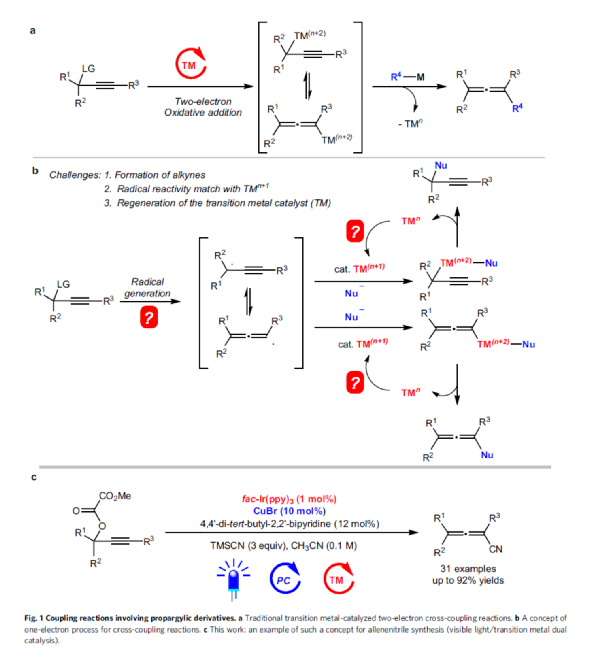
聯(lián)烯結(jié)構(gòu)單元廣泛存在于天然產(chǎn)物、生物活性分子和功能材料中。目前,化學家們已報道了多種合成聯(lián)烯化合物的方法,如2-鹵代-1,3-丁二烯或聯(lián)烯基酯的聯(lián)烯基取代反應、1,3-烯炔的1,4-雙官能團化反應、末端炔烴的聯(lián)烯基化反應以及涉及炔丙基底物的偶聯(lián)反應等。其中,在炔丙基底物的偶聯(lián)反應中,過渡金屬催化的炔丙基醇衍生物與有機金屬試劑的偶聯(lián)反應涉及雙電子的氧化加成-轉(zhuǎn)金屬化-還原消除的過程(Fig. 1a)。然而,由于固有的雙電子機理,導致反應的適用范圍與選擇性較低。并且,聯(lián)烯腈是有機合成中有價值的前體化合物,而經(jīng)典的通過對炔丙醇底物氰化反應合成該類化合物的方法中需要使用當量的CuCN,炔丙醇,高達1.5當量的劇毒KCN,以及2.5當量的HBr。麻生明院士團隊設(shè)想,是否可通過涉及單電子過程的炔丙基衍生物的偶聯(lián)反應直接合成聯(lián)烯腈化合物(Fig. 1b)。該策略存在如下可能的挑戰(zhàn),(1)可能形成炔烴產(chǎn)物的區(qū)域選擇性問題;(2)自由基反應性與過渡金屬配合物活性的匹配問題;(3)過渡金屬催化劑的再生循環(huán)問題。在此,上海有機所麻生明院士團隊報道了一種新型的光催化劑/銅催化劑雙重催化炔丙基草酸酯與TMSCN的氰化反應,從而合成了一系列多取代聯(lián)烯腈衍生物(Fig. 1c)。
(圖片來源: Nat. Commun.)
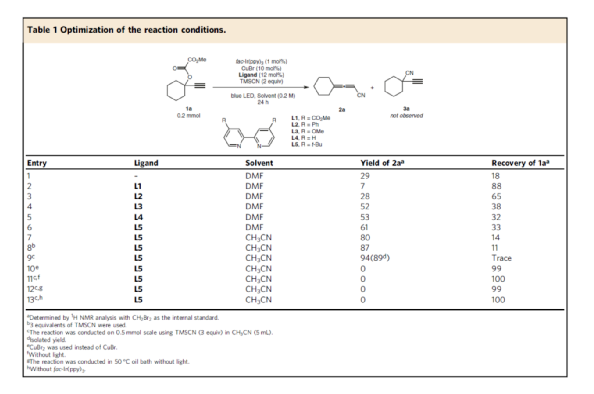
首先,作者以炔丙基草酸酯1a作為模型底物,進行了相關(guān)氰化反應條件的篩選(Table 1)。發(fā)現(xiàn)當以CuBr作為金屬催化劑,fac-Ir(ppy)3作為光催化劑,L5作為配體,TMSCN作為氰源,在乙腈中于藍色LED照射下反應,能以94%的收率獲得產(chǎn)物2a。
(圖片來源: Nat. Commun.)
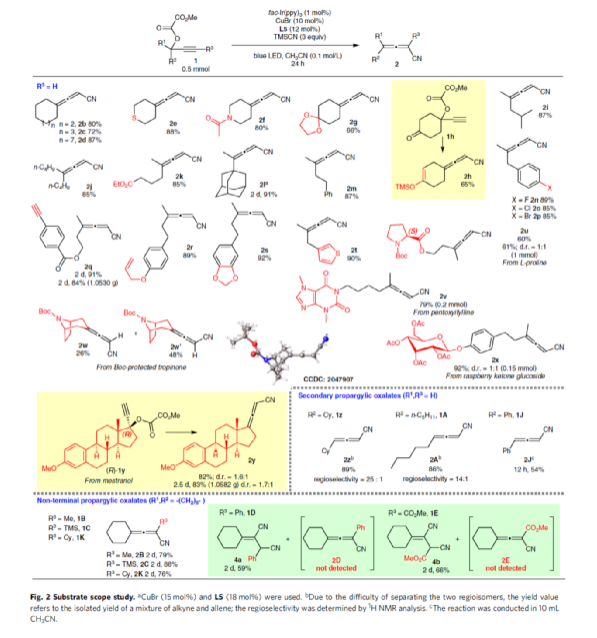
在獲得上述最佳反應條件后,作者對底物范圍進行了擴展(Fig. 2)。首先,環(huán)狀(2a,2b,2c,2d)和非環(huán)狀(2i,2j,2m)底物,都可以實現(xiàn)良好的收率。而即便對于大位阻的含有金剛烷基取代的底物1l,只需要將CuBr和L5的用量稍加提高,便可順利的以91%收率得到產(chǎn)物2l。值得注意的是,一些活性的官能團(如鹵素、酯基、炔基、烯基等),均與體系兼容。有意思的是,在標準條件下,含有酮羰基的炔丙基草酸酯1h可轉(zhuǎn)化為具有烯醇硅基醚單元的產(chǎn)物2h,收率為65%。對于含有噻吩基取代的1t,同樣適用,可以以90%收率得到產(chǎn)物2t。此外,該策略還成功用于了對一些具有生物活性的分子的后期修飾中,如L-脯氨酸衍生物(2u)、己酮可可堿衍生物(2v)、Boc-保護的托品酮(2w和2w')、覆盆子酮葡萄糖苷衍生物(2x)、美雌醇(2y)等。該反應也可以順利的在克級規(guī)模上實現(xiàn),如2q和2y。即使對于末端二級炔丙基草酸酯1z和1A,也可獲得良好收率的相應1,3-二取代聯(lián)烯產(chǎn)物2z和2A,具有出色的化學選擇性。4-苯基聯(lián)烯腈產(chǎn)物2J也可通過該策略獲得。此外,該策略的底物范圍可進一步擴展到非末端炔丙基草酸酯,如1B、1C和1K。然而,當?shù)孜镏械腞3為-Ph和 -CO2Me時,反應單一得到了二腈類化合物4a和4b,這可能是由于TMSCN與原位形成的聯(lián)烯腈中間體2D和2E的共軛加成導致。
(圖片來源: Nat. Commun.)
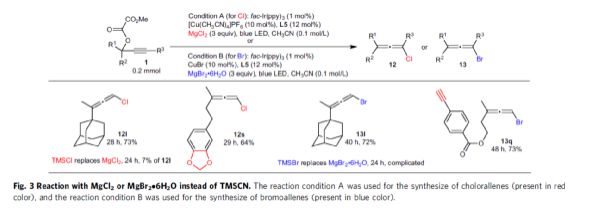
緊接著,作者發(fā)現(xiàn),當使用MgCl2或MgBr2?6H2O代替TMSCN作為親核試劑時,反應也可以順利地得到相應的氯代聯(lián)烯12l、12s或溴代聯(lián)烯13l、13q,收率為64-73%。然而,當使用TMSBr或TMSCl時,反應的效果較差(Fig. 3)。
(圖片來源: Nat. Commun.)
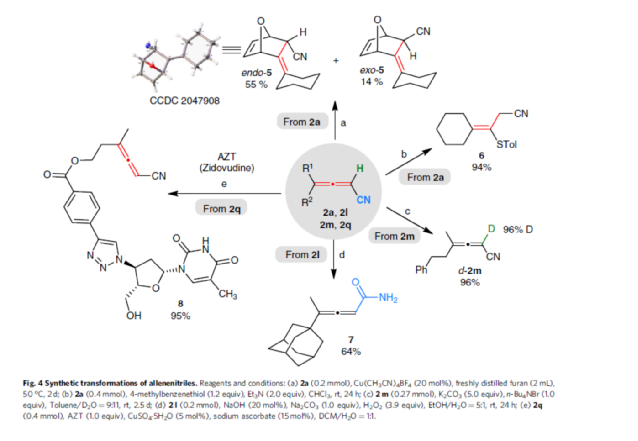
隨后,作者對反應的實用性進行了研究(Fig. 4)。首先,Cu(I)-催化2a與呋喃的[4+2]環(huán)加成反應,可以分別以55%和14%的收率得到氧雜橋環(huán)化合物endo-5以及exo-5。4-甲基苯硫醇與2a的共軛加成,可以以優(yōu)異的收率得到硫代四取代烯烴6。其次,在K2CO3和n-Bu4NBr存在下,用D2O對2m的α-H進行直接氘代可以方便的得到氘代聯(lián)烯產(chǎn)物d-2m,收率為96%,氘代率為96%。2l中的腈基可在堿性條件下進行水解,以64%收率的聯(lián)烯基酰胺化合物7。此外,2q中的乙炔基可與抗HIV藥物AZT(齊多夫定)進行銅催化的點擊反應,而聯(lián)烯腈單元保持完整,為進一步衍生化提供了可能。
(圖片來源: Nat. Commun.)
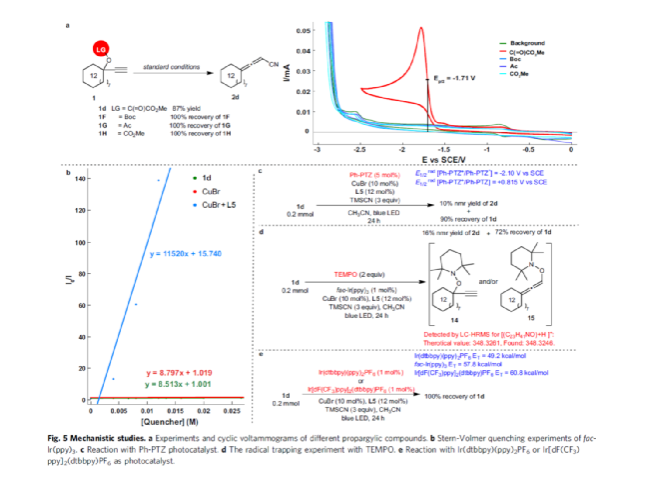
作者還對反應機理進行了進一步的研究(Fig. 5)。首先,作者制備了幾種帶有不同離去基團的炔丙基化合物1F、1G和1H,通過CV實驗表明,這些基團是氧化還原非活性的離去基團(Fig. 5a)。隨后,通過fac-Ir(ppy)3的Stern-Volmer淬滅實驗發(fā)現(xiàn),fac-Ir(ppy)3的激發(fā)態(tài)可被CuBr/L5催化劑有效地淬滅(Fig. 5b)。同時,作者分析如果反應按照光催化的氧化淬滅循環(huán)進行,那么Ph-PTZ則可以作為另一種可能的光催化劑用于該反應,(在Ph-PTZ存在下反應很容易生成自由基10或11,Ph-PTZ+的氧化態(tài)和LCuICN之間的后續(xù)單電子轉(zhuǎn)移過程形成LCuIICN,可進一步轉(zhuǎn)化為2d)。然而,實際反應中僅以10%收率得到2d,同時原料1d的回收率為90%(Fig. 5c)。此外,當在1d的標準反應體系中加入TEMPO時,反應顯著受到抑制,并通過LC-HRMS觀察到TEMPO加合物14或15的生成,從而表明反應涉及自由基的機理(Fig. 5d)。最后,當使用三線態(tài)能量與fac-Ir(ppy)3接近的Ir(dtbbpy)(ppy)2PF6或Ir[dF(CF3)ppy]2(dtbbpy)PF6作為光催化劑時,反應均未能順利發(fā)生,進一步排除了能量轉(zhuǎn)移的機理(Fig. 5e)。
(圖片來源: Nat. Commun.)
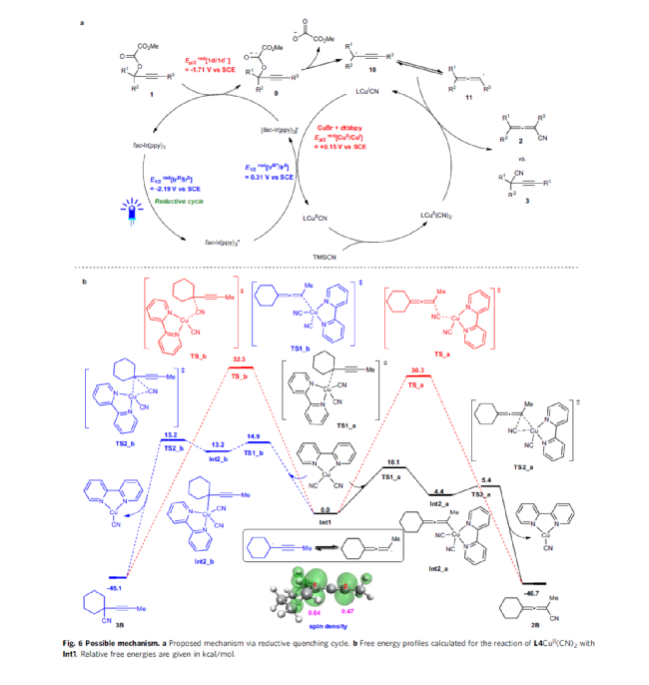
基于上述的研究以及相關(guān)DFT計算的研究,作者提出了一種合理的催化循環(huán)過程(Fig. 6a)。首先,在光催化劑的還原淬滅循環(huán)中,fac-Ir(ppy)3*的激發(fā)態(tài)被LCuICN 淬滅,生成了LCuII(CN)和[fac-Ir(ppy)3]-物種。隨后,底物1可被[fac-Ir(ppy)3]-還原,經(jīng)單電子還原過程生成陰離子自由基中間體9,中間體9離去草酸酯陰離子后形成炔丙基自由基中間體10。該中間體可以異構(gòu)化為聯(lián)烯基自由基11,可與LCuII(CN)反應經(jīng)還原消除,生成聯(lián)烯產(chǎn)物2并再生催化活性物種LCuICN。同時,作為另一種可能的反應途徑,11也可能從LCuII(CN)2中直接攫取氰基,生成聯(lián)烯產(chǎn)物2。底物中的R1、R2和R3的空間位阻效應可能在形成2或3的反應選擇性中起著重要的作用。
(圖片來源: Nat. Commun.)
總結(jié):上海有機所麻生明院士團隊報道了一種新型可見光參與的銅催化炔丙基草酸酯與TMSCN的氰化反應,從而合成了一系列多取代聯(lián)烯腈衍生物,具有反應條件溫和、底物范圍廣泛、官能團兼容性高、化學與區(qū)域選擇性出色等特點。機理研究表明,光誘導單電子過程生成的炔丙基自由基和聯(lián)烯基自由基通過光催化劑的還原淬滅循環(huán)參與了反應,而非傳統(tǒng)過渡金屬催化的雙電子氧化加成過程。
參考資料:https://mp.weixin.qq.com/s/oDFaY7TAYDylPNWKhsp_iw
聲明:化學加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權(quán)益,請作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn