(圖片來源:Angew. Chem. Int. Ed.)
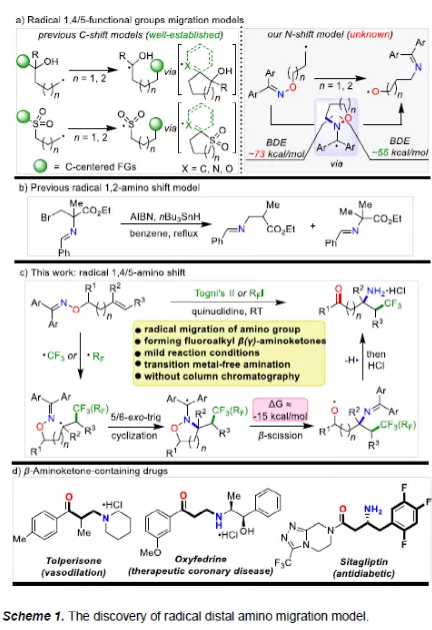
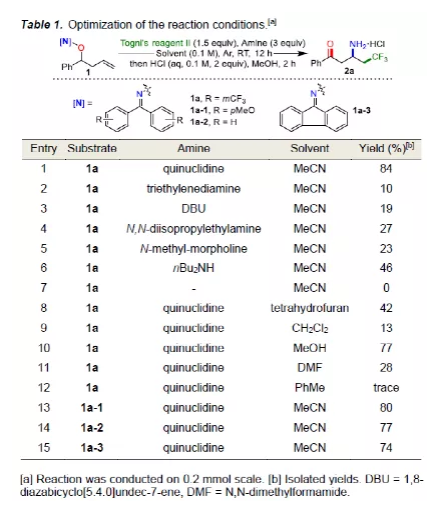
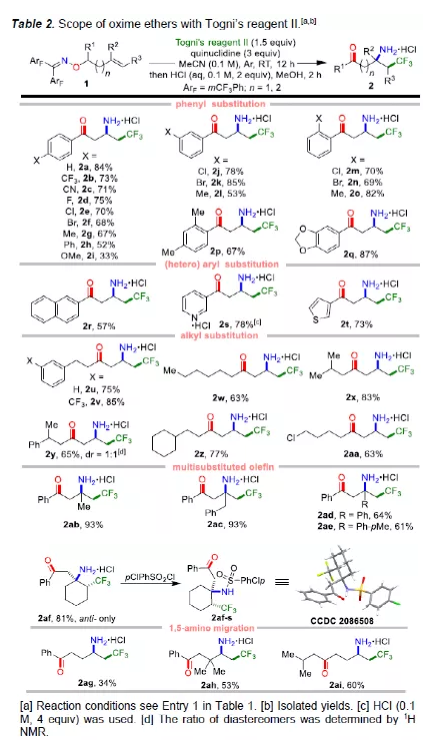
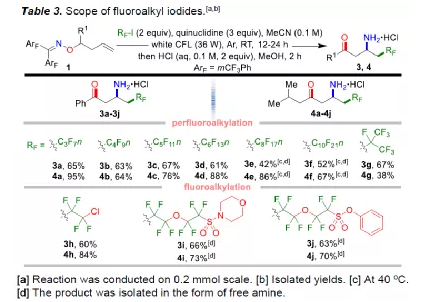
自由基遷移反應,尤其是遠程遷移,可在遠端位置輕松引入官能團(FGs),是構建復雜分子的有效策略。對于使用特定結構的醇或Smiles重排,烯基、羰基、炔基、氰基和(雜)芳基的自由基1,4-/1,5-遷移已被廣泛應用于有機合成(Scheme 1a, left)。盡管在以碳為中心FGs的遠程遷移方面已取得一定的成果,但對于以雜原子為中心的FGs自由基遷移卻受到了限制。肟醚是一種易得的化合物,它在自由基反應中的應用主要集中在N-O鍵斷裂生成亞胺基自由基。作者假設,如果一個碳自由基以快速5/6-exo-trig環化到酮肟醚C=N雙鍵的N原子上,通過利用C-N和N-O鍵之間的鍵解離能(BDE)差異作為熱力學驅動力,那么形成的碳中心自由基很可能在弱N-O鍵處發生β-斷裂,生成一個氧中心自由基(Scheme 1a, right)。然而,對于以氮為中心的FGs的由基遷移卻很少被探索。1990年,Frey課題組提出了一種化學1,2-亞胺遷移的模型,然而尚未實現遠程自由基氨基遷移(Scheme 1b)。在此,韓丙教授課題組提出了一種新型的自由基1,4/5-氨基轉移反應。該反應使用烯烴衍生的二苯基酮肟醚作為底物,由Togni's試劑II/全氟烷基碘和奎寧環的電子供體-受體(EDA)配合物衍生的氟烷基自由基觸發反應。通過遷移和酸性水解,首次有效地合成了多種氟烷基一級β(γ)-氨基酮衍生物(Scheme 1c)。值得注意的是,該策略代表了第一個自由基1,4/5-氨基轉移的例子。此外,氨基酮和氟化氨基酮廣泛存在于藥物中,并具有多種重要的生物活性(Scheme 1d)。下載化學加APP,閱讀更有效率。(圖片來源:Angew. Chem. Int. Ed.)首先,作者化合物1作為模型底物,對胺和溶劑進行了篩選(Table 1)。反應的最佳條件為:先將Togni's試劑II,化合物1a與奎寧環(胺源)于MeCN溶劑中室溫攪拌12 h,再通過HCl水解,即可獲得84%收率的三氟甲基取代的一級β-氨基酮鹽酸鹽2a(圖片來源:Angew. Chem. Int. Ed.)在獲得上述最佳條件后,作者對底物范圍進行了擴展(Table 2)。當底物中的R1取代為各種芳香族取代基、雜芳基取代基和烷基取代基時,均可順利反應,獲得相應的產物2a-2aa。其次,當底物中的R2和R3取代為烷基或取代的芳基時,也可獲得相應的產物2ab-2ae。對于環狀底物1af,以81%的收率獲得區域選擇性和立體選擇性三氟甲基β-氨基酮2af,其構型是通過磺酰基衍生物2af-s的單晶X-射線確認。值得注意的是,使用酮肟醚底物1ag-1a,在標準條件下可進行1,5-氨基遷移,從而獲得三氟甲基取代的γ-氨基酮2ag-2ai。下載化學加APP,閱讀更有效率。(圖片來源:Angew. Chem. Int. Ed.)除了Togni’s試劑II外,作者還對其它廉價的全氟烷基碘進行了探索(Table 3)。一系列全氟烷基碘均可在36 W的CFL照射條件下順利反應,獲得相應的產物3a-3j和4a-4j,收率為38-95%。值得注意的是,可見光照射對于全氟烷基碘化物至關重要,可能是由于它們與奎寧環形成的EDA配合物的穩定性高,需要額外的能量才能激發成相應的電子轉移(ET)配合物。(圖片來源:Angew. Chem. Int. Ed.)隨后,通過兩步簡單的操作,可直接實現2a(收率為75%)和2x(收率為84%)的克級規模放大,進一步證明了反應的實用性(Scheme 2)。(圖片來源:Angew. Chem. Int. Ed.)此外,作者還對反應的機理進行了研究(Scheme 3)。首先,當體系加入奎寧環后,在UV分析中Togni’s試劑II和nC4F9I均發生紅移,在核磁共振滴定實驗中Togni’s試劑II和nC4F9I的19F NMR信號峰向高場移動。同時,電子順磁共振(EPR)實驗表明,這種EDA配合物中產生了三氟甲基自由基,可以被α-苯基-N-叔丁基硝酮捕獲。上述結果表明,EDA配合物是由奎寧環和Togni’s試劑II/氟代烷基碘之間的鹵代鍵相互作用形成并引發自由基反應(Schemes 3a-3c)。其次,1a在標準條件下反應時(未進行水解),可形成相應的1,4-亞氨基遷移產物2a’,當向反應體系中加入TEMPO時,則反應完全被抑制。當使用1aj為底物時,在標準條件下(未進行水解)獲得46%收率的產物2aj',且形成13%收率的去異丙基產物2aj''。上述結果表明,2aj''源自氧中心自由基的β斷裂形成,這無疑源自自由基1,4-氨基遷移(Scheme 3d)。此外,作者還通過密度泛函理論(DFT)計算對反應機理進行了進一步的研究(Scheme 3e)。基于上述的討論,作者提出了一種可能的反應機理(Scheme 3f)。首先,Togni’s試劑II或氟代烷基碘與奎寧環通過鹵素-鍵相互作用形成EDA配合物,通過自發或白光誘導過程轉化為相應的ET產物,即CF3/氟烷基自由基和奎寧環自由基陽離子。其次,原位生成的CF3或氟烷基自由基進攻酮肟醚1中的C=C鍵,產生碳自由基I。隨后,碳自由基I發生動力學上有利的5(6)-exo-trig環化以生成中間體II,中間體II通過N-O鍵的斷裂和1,4(5)-N-遷移形成相應的氧自由基III。最后,氧自由基III與奎寧環自由基陽離子經HAT氧化形成氟代烷基取代的β(γ)-亞氨基酮,再經水解即可獲得最終產物2-4。(圖片來源:Angew. Chem. Int. Ed.)基于對反應機理的理解,作者還使用其它的EDA受體來進一步探索該反應的適用性(Table 4)。反應結果表明,芳基/烷基磺甲基、三氯甲基、烷基等缺電子/富電子的自由基,甚至疊氮自由基,均與該體系兼容,以高產率獲得相應的功能化β-氨基酮5a-5l。(圖片來源:Angew. Chem. Int. Ed.)總結:蘭州大學韓丙課題組首次報道了一種溫和且高效的自由基1,4/5-氨基轉移策略,可實現底物中氧原子到碳原子的遷移。同時,該策略利用快速5(6)-exo-trig自由基環化和弱N-O鍵斷裂作為動力學和熱力學驅動力,并利用適當自由基前體和奎寧環的氧化還原作為自由基引發步驟。因此,在無金屬條件下有效地合成了一系列結構重要且具價值的功能化一級β(γ)-氨基酮衍生物。