




近二十年,腫瘤免疫治療被認(rèn)為是治療晚期和轉(zhuǎn)移性腫瘤最有效的新方法之一,該療法通過(guò)緩解腫瘤微環(huán)境的免疫抑制現(xiàn)象,刺激機(jī)體免疫系統(tǒng)的抗腫瘤活力,從而取得顯著療效。但是許多腫瘤細(xì)胞在免疫逃逸的過(guò)程中通常表現(xiàn)為低抗原性,使得體內(nèi)免疫細(xì)胞難以識(shí)別腫瘤抗原而發(fā)揮療效。近十年的研究顯示,一些抗癌藥物或物理手段不僅能殺死腫瘤細(xì)胞,還會(huì)促進(jìn)腫瘤抗原的暴露,提高腫瘤細(xì)胞的免疫原性,有利于免疫系統(tǒng)的識(shí)別,這一現(xiàn)象被稱為免疫原性細(xì)胞死亡(ICD)。然而,腫瘤細(xì)胞在發(fā)生ICD的同時(shí),會(huì)伴隨大量ATP的釋放,當(dāng)其被胞外核苷酶代謝后,最終會(huì)生成大量腺苷(ADO),與廣泛存在于各種免疫細(xì)胞表面的2A型腺苷受體(A2AR)結(jié)合后,激活免疫細(xì)胞的免疫抑制通路,加劇腫瘤免疫抑制微環(huán)境。因此,ICD誘導(dǎo)的抗腫瘤免疫和ADO介導(dǎo)的免疫抑制之間的矛盾是一個(gè)巨大的挑戰(zhàn)。
杜永忠教授致力于新型納米給藥系統(tǒng)的開發(fā)及腫瘤靶向免疫治療研究,課題組近年來(lái)在Angewandte Chemie International Edition、Nano Letters、Biomaterials、 Journal of Controlled Release、ACS Applied Materials & Interface等國(guó)際著名期刊發(fā)表多項(xiàng)原創(chuàng)性工作。本研究在前期工作的基礎(chǔ)上,針對(duì)上述矛盾,設(shè)計(jì)了一種共載ICD誘導(dǎo)劑阿霉素和A2AR拮抗劑SCH 58261的溫敏性膠束,并在表面修飾E-選擇素,靜脈注射后可在E-選擇素的介導(dǎo)下粘附在白細(xì)胞的表面,隨白細(xì)胞一同遷移至腫瘤部位,實(shí)現(xiàn)納米粒的腫瘤高度富集,還解決了人工合成納米粒易被網(wǎng)狀內(nèi)皮系統(tǒng)捕獲、難以穿透生物屏障等問(wèn)題。
研究結(jié)果表明,E-選擇素修飾的載藥膠束靜脈注射后,可在血液循環(huán)中迅速粘附于白細(xì)胞表面,通過(guò)“搭乘白細(xì)胞的便車”實(shí)現(xiàn)腫瘤高效靶向。積累在腫瘤部位的載藥膠束在局部微波熱療的刺激下實(shí)現(xiàn)藥物的快速釋放,所釋放的阿霉素在阻滯腫瘤細(xì)胞周期的同時(shí),還可以誘導(dǎo)腫瘤發(fā)生ICD,激活機(jī)體的腫瘤特異性細(xì)胞免疫,而SCH 58261通過(guò)有效拮抗各種免疫細(xì)胞表面的A2AR,緩解腫瘤免疫抑制微環(huán)境,最終實(shí)現(xiàn)化療和免疫治療的協(xié)同抗腫瘤作用。
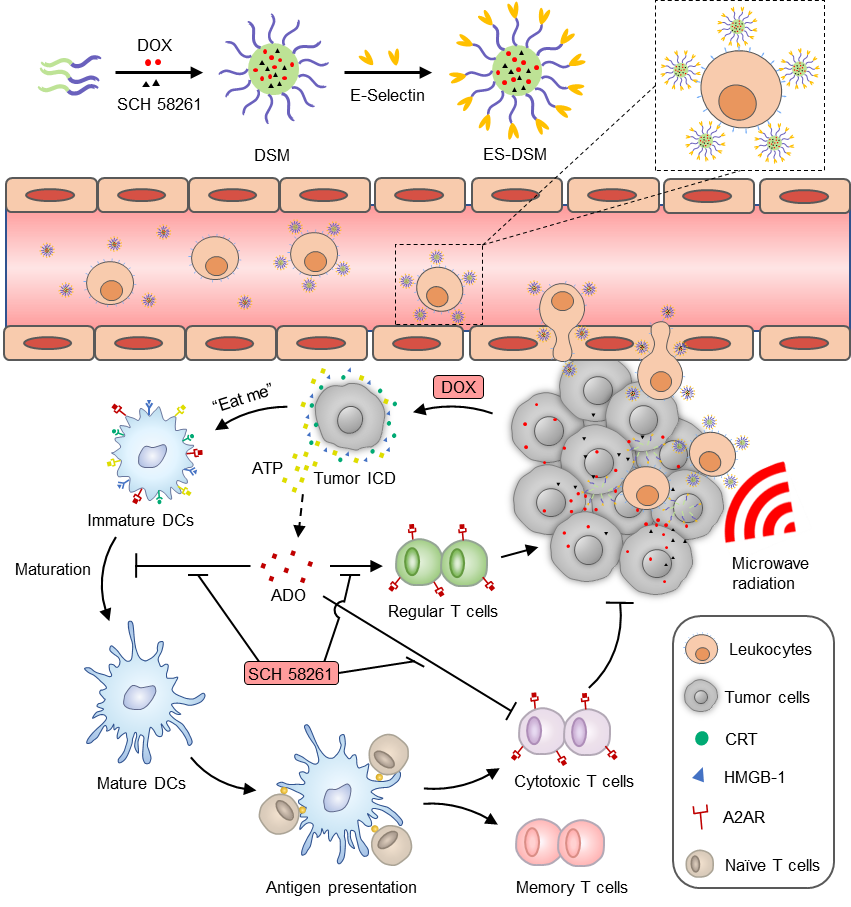
本研究利用溫敏性膠束共載ICD誘導(dǎo)劑和A2AR拮抗劑,利用白細(xì)胞為運(yùn)載工具,實(shí)現(xiàn)藥物的腫瘤高效靶向,在提高腫瘤免疫原性的同時(shí),緩解免疫抑制微環(huán)境,為腫瘤治療提供了一種雙管齊下的策略。
本課題受到國(guó)家重點(diǎn)研發(fā)計(jì)劃“政府間國(guó)際科技創(chuàng)新合作”項(xiàng)目和浙江省自然科學(xué)基金重大項(xiàng)目的支持。本文第一作者為2016級(jí)博士生祁菁和2017級(jí)博士生金斐旸,通訊作者為我院杜永忠教授和徐曉玲博士、浙大麗水醫(yī)院紀(jì)建松教授和浙大醫(yī)學(xué)院附屬第一醫(yī)院吳李鳴教授。
參考資料:http://www.cps.zju.edu.cn/2021/0812/c26425a2414842/page.htm
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來(lái)源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn