

前列腺素(Prostaglandin, PG)是一類廣泛存在于體內的自體活性物質,介導體內多種生理功能。前列腺素類化合物具有非常高的成藥性,目前,在全球范圍內有超過20種前列腺素類上市藥物。由于前列腺素類化合物獨特的結構和廣泛的生物活性,發展前列腺素的高效合成方法具有非常重要的意義。在過去的50多年間,前列腺素一直是合成化學家的重要目標分子。
南方科技大學化學系講席教授張緒穆、前沿與交叉科學研究院研究副教授陳根強團隊以自主開發的烯炔環異構化反應和不對稱氫化反應為關鍵步驟實現了前列腺素類化合物的高效不對稱合成,極大地提高了合成效率。相關研究成果以“Concise, scalable and enantioselective total synthesis of prostaglandins”為題,于北京時間2021年5月27日發表在Nature Chemistry。
1934年,前列腺素被von Euler等學者首次發現,當時認為此物質可能是由前列腺所分泌,因此命名為前列腺素。1957年Bergstr?m及其瑞典同事Samuelsson分離出了PGF1和PGF2α的純品,并在后續研究中闡明了前列腺素的結構和代謝過程,有關前列腺素藥物的研究在隨后的20世紀60年代達到高潮。1982年,Bergstr?m與Samuelsson和John Vane三位科學家因在前列腺素及有關生物活性物質的研究方面的卓越貢獻共同獲得了諾貝爾生理學和醫學獎。
PGF2α是前列腺素家族中最復雜的化合物,其核心結構為具有四個連續手性中心的環戊烷骨架和兩個側鏈(圖1a)。1964年,E. J. Corey首次實現了PGF2α的全合成,隨后,許多著名的有機化學家如Woodward、Stork、Noyori、Danishefsky、Aggarwal、Baran、Grubbs、陳芬兒等也在前列腺素的合成方面作出了許多重要的研究工作。盡管前列腺素的合成取得了重要進展,已經開發了多條合成路線,但是,這些已有的合成路線不適用于工業化合成,目前前列腺素類藥物的工業合成仍然依賴Corey內酯(10),Corey內酯可以從環戊二烯9出發經過9步合成得到,從Corey內酯出發仍需要多步反應才能夠得到前列腺素,有些前列腺素分子甚至需要超過10步來合成(圖1b)。在該研究工作中,團隊設計合成了一個合成前列腺素的關鍵中間體15,從該中間體出發僅需要兩步就可以合成得到前列腺素化合物,該中間體可以通過簡單易得的β-酮酰胺11經過4步合成得到(圖1c)。
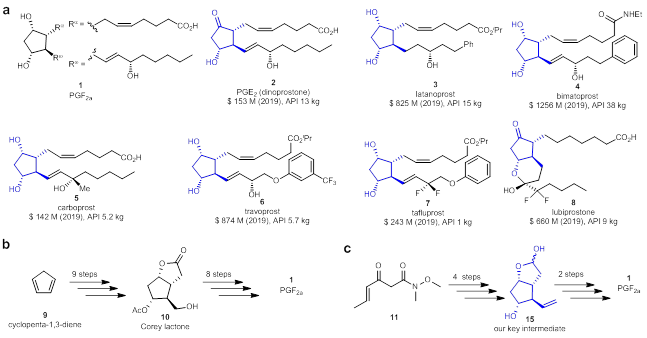
圖1 a. 一些代表性的前列腺素類藥物的結構;b. Corey小組前列腺酸的合成方法(Corey內酯為關鍵中間體);c. 張緒穆團隊開發的前列腺素的合成方法(化合物15為關鍵中間體)
前列腺素不對稱合成中的主要難點在于其核心環戊烷骨架中四個連續手性中心的精準構建以及兩個側鏈的高效引入。2000年,張緒穆研究團隊報道了首例銠催化的1,6-烯炔的環異構化反應,可以實現手性五元環化合物的高效構建,對于大多數底物,采用常見的BINAP作為手性配體,該反應就可以獲得非常高的對映選擇性。2014,該反應被人名反應收錄(張-烯炔環異構化反應),成為為數不多的幾個以華人姓氏命名的人名反應(Li, J. J. Zhang enyne cycloisomerization in Name Reactions: A Collection of Detailed Mechanisms and Synthetic Applications 652–653, Springer, 2014) (圖2)。2016年,張緒穆研究團隊設計合成了一個基于二茂鐵骨架的手性三齒配體f-amphox (L1), 該配體與銥的絡合物在簡單酮的不對稱氫化中表現出優異的活性和対映選擇性(up to 1,000,000 TON, up to >99% ee),甚至在無溶劑條件下反應也能夠高效進行(Org. Lett. 2016, 18, 2938-2941)。
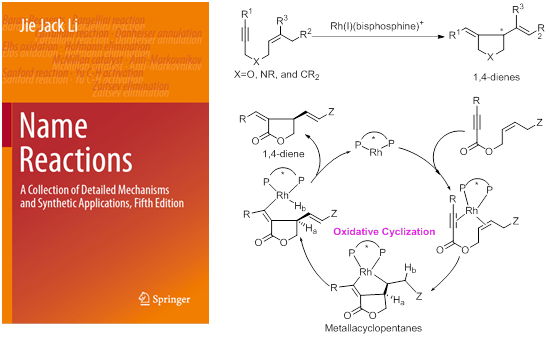
圖2 張-烯炔環異構化反應及其機理
研究團隊設想以銠催化的不對稱烯炔環異構化反應為關鍵步驟構建手性環戊烷骨架,進而實現前列腺素PGF2α的不對稱合成。他們對前列腺素PGF2α進行了逆合成分析(圖3),發現目標化合物PGF2α (1)可以通過關鍵中間體15,經過Grubbs烯烴交叉復分解反應和Wittig反應合成得到,而關鍵中間體15則可以通過1,6-烯炔底物13的不對稱環異構化反應和后續的還原得到,1,6-烯炔底物13可以通過化合物12和化合物18的鋰鹽的加成反應合成得到,化合物12則可以通過簡單易得的β-酮酰胺11的不對稱氫化和現場硅基保護得到。
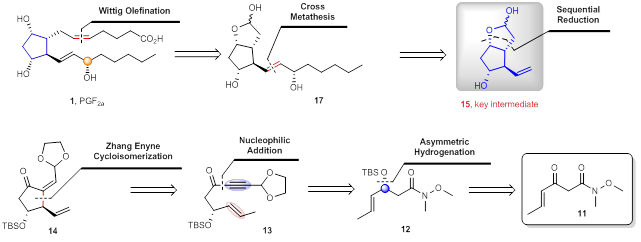
圖3 前列腺素的逆合成分析
基于上述逆合成分析,團隊以β-酮酰胺11為起始原料,對前列腺素PGF2α的合成進行了探索(圖4)。采用張緒穆研究團隊前期開發的f-amphox (L1)為手性配體,β-酮酰胺11在銥催化下可以被對映選擇性還原并以70%的收率和94%的對映選擇性得到化合物12,化合物12中的Weinreb酰胺可以和化合物18的鋰鹽發生加成反應順利轉化為1,6-烯炔化合物13。以銠為催化劑以及(S)-BINAP為手性配體,1,6-烯炔化合物13發生不對稱烯炔環異構化反應,能夠以85%的收率、98%的對映選擇性和>20/1的非對映選擇性得到化合物14。化合物14中的共軛雙鍵和羰基可以分別被二苯基硅氫和三乙基硼氫化鋰還原,通過調節還原產物的后處理方式可以選擇性地得到關鍵中間體15或16。中間體16的穩定性大于中間體15,中間體16在鹽酸的處理下也可以轉化為中間體15。
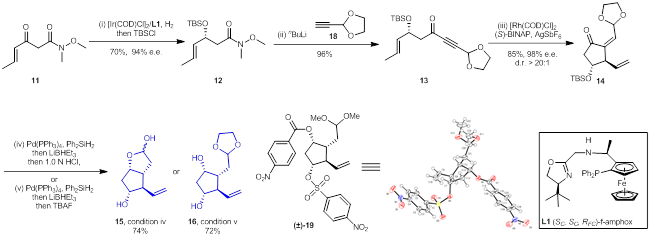
圖4 前列腺素關鍵中間體15和16的高效合成
在順利合成得到關鍵中間體15后,團隊對前列腺素的最終合成進行了嘗試(圖5)。關鍵中間體15在Hoveyda-Grubbs二代催化劑的作用下可以和手性醇中間體19發生Grubbs交叉復分解反應順利得到化合物17,化合物17再經過一步經典的Wittig反應就可以15%的總收率順利得到前列腺素PGF2α (1)。采用類似的合成路線,拉坦前列素 (latanoprost, 3)、卡波前列素 (carboprost, 5)和氯前列烯醇(cloprostenol, 22)也能夠分別以5.7%、23%以及19%的總收率分別合成得到。值得一提的是,氟前列醇(fluprostenol, 23)可以以27%的總收率和23克的規模合成得到,氟前列醇(fluprostenol, 23)經過一步酯化反應就可以得到曲伏前列素(travoprost, 6)。此外,地諾前列酮(dinoprostone, 2)也可以從化合物11出發經過7步反應形式合成得到。
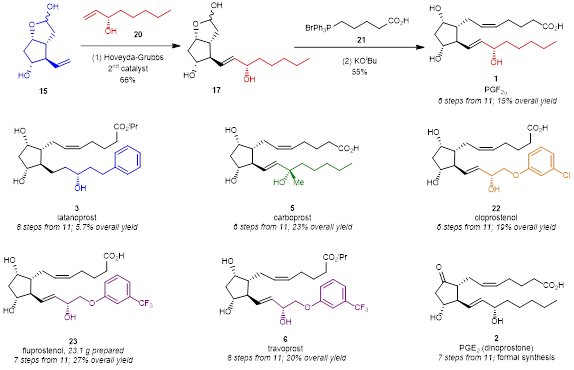 圖5 前列腺素的最終合成
圖5 前列腺素的最終合成
最后,張緒穆、陳根強研究團隊設計、合成了一種合成前列腺素的關鍵中間體15和16,并以自主開發的烯炔環異構化反應和不對稱氫化為關鍵步驟實現了該中間體的高效合成。基于該中間體僅需要兩步就可以合成得到前列腺素化合物。該合成方法具有原子經濟性、步驟經濟性和氧化還原經濟性等特點,為前列腺素相關藥物的合成提供了極大的便利,不僅可以有效降低前列腺素相關藥物的生產成本而且對前列腺素相關藥物的研發具有非常重要的意義。
張緒穆和陳根強為本論文共同通訊作者,張緒穆和新加坡國立大學教授盧一新的2017級聯合培養博士研究生張芙豪為本文第一作者。南科大為論文第一單位。
該項研究工作得到了國家自然科學基金、廣東省重點領域研發計劃項目、廣東省普通高校創新團隊、深圳市科技創新委員會、深圳市諾獎實驗室等項目的資金支持。
論文鏈接:
https://www.nature.com/articles/s41557-021-00706-1
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn