



研究目的:發(fā)展全新的合成方法,實(shí)現(xiàn)天然產(chǎn)物和藥物分子“優(yōu)勢(shì)骨架”α-亞甲基-g-丁內(nèi)酯(α-methylene-g-butyrolactone,MBL)的多樣性和可控性合成
α-亞甲基-g-丁內(nèi)酯(α-methylene-g-butyrolactone,MBL)是有機(jī)化合物中一種重要的結(jié)構(gòu)單元,廣泛存在于眾多活性天然產(chǎn)物以及藥物分子結(jié)構(gòu)中。作為一種Michael反應(yīng)受體,α-亞甲基-g-丁內(nèi)酯可與生物大分子通過1,4-共軛加成反應(yīng)形成共價(jià)鍵,進(jìn)而影響其生理功能,被視為一類具有共價(jià)結(jié)合模式的“藥效團(tuán)”。傳統(tǒng)構(gòu)建此類化合物的方法在產(chǎn)物結(jié)構(gòu)多樣性和化學(xué)、立體選擇性控制方面存在不足之處,因此發(fā)展新穎高效、精準(zhǔn)可控的合成方法解決此類化合物的多樣性合成問題具有重要的研究和應(yīng)用價(jià)值。
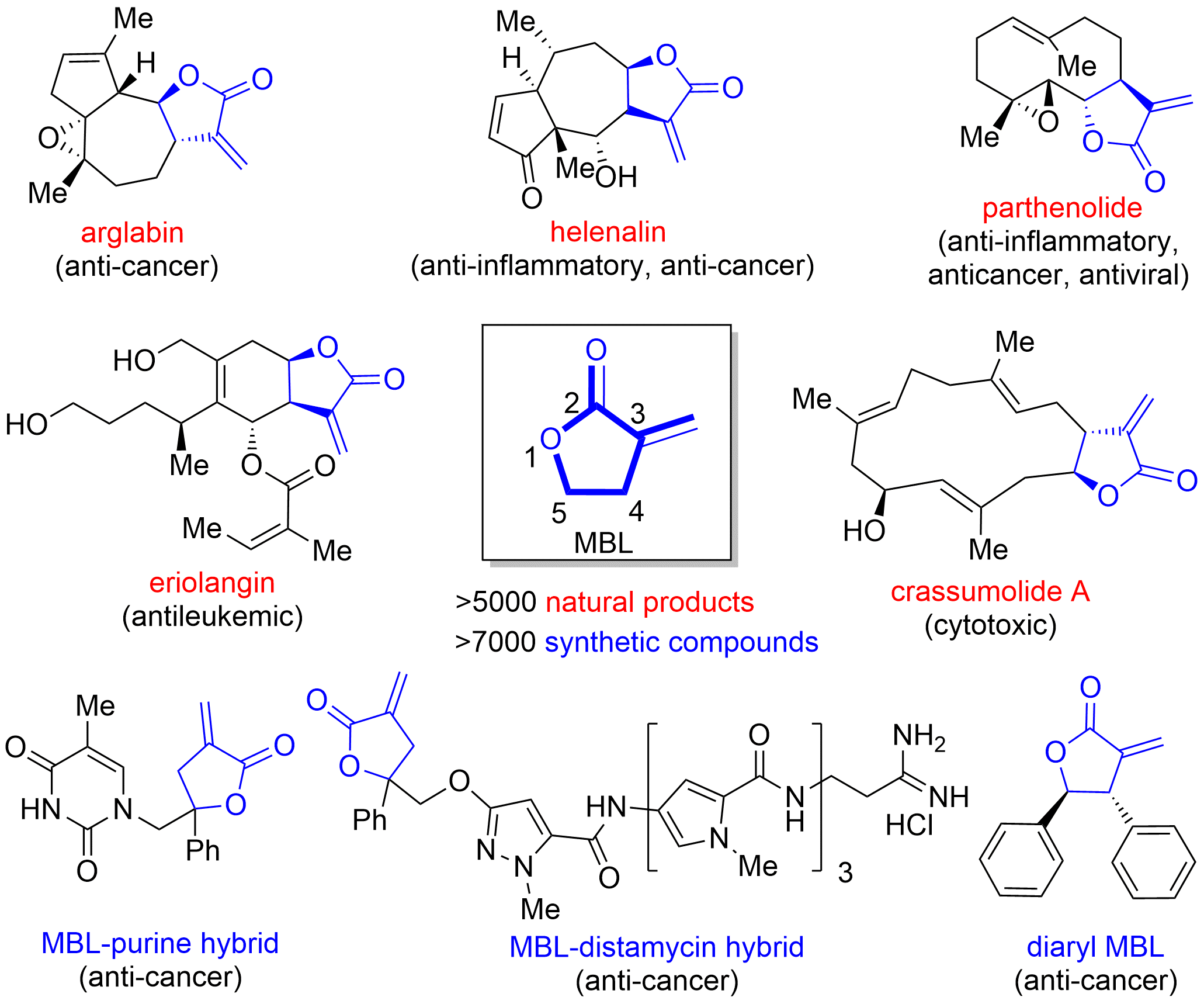
圖1.含有α-亞甲基-g-丁內(nèi)酯結(jié)構(gòu)單元的一些重要天然產(chǎn)物和活性分子
研究階段一:dyotropic重排反應(yīng)的難點(diǎn)突破
唐葉峰課題組長(zhǎng)期致力于dyotropic重排反應(yīng)研究,并將其應(yīng)用于活性天然產(chǎn)物合成。2012年,該課題組報(bào)道了3,4-順式二取代- b-環(huán)丙內(nèi)酯dyotropic重排反應(yīng),并將其應(yīng)用于蒼耳烷倍半萜類天然產(chǎn)物全合成(Angew. Chem. Int. Ed. 2012, 51, 6984–6988)。在此基礎(chǔ)上,本項(xiàng)研究將該反應(yīng)擴(kuò)展到另一類更具挑戰(zhàn)性的底物,即α-亞甲基-b-環(huán)丙內(nèi)酯。此類底物的dyotropic重排反應(yīng)之前從未有人報(bào)道,主要是存在以下難點(diǎn):1)底物具有高環(huán)張力和高度官能團(tuán)化的特點(diǎn),易發(fā)生一些潛在的副反應(yīng),如酰基C-O鍵或烷基C-O鍵斷裂開環(huán)反應(yīng),Michael 加成反應(yīng)和脫CO2反應(yīng);2)該類底物構(gòu)象靈活,即使發(fā)生dyotropic重排反應(yīng),遷移基團(tuán)的化學(xué)選擇性(如氫遷移或碳遷移)較難控制,存在不確定性。
通過系統(tǒng)優(yōu)化反應(yīng)條件,唐葉峰課題組順利實(shí)現(xiàn)了α-亞甲基-b-環(huán)丙內(nèi)酯dyotropic重排反應(yīng)。研究表明,該反應(yīng)具有廣泛的底物適用性,可適用于不同取代類型的α-亞甲基-b-環(huán)丙內(nèi)酯。尤為重要的是,反應(yīng)中遷移基團(tuán)的遷移順序表現(xiàn)出一定的規(guī)律性(芳基>氫>烷基),因此反應(yīng)產(chǎn)物取代類型和立體化學(xué)可調(diào)可控。計(jì)算化學(xué)和實(shí)驗(yàn)證據(jù)表明,該反應(yīng)很可能是通過協(xié)同異步的機(jī)理進(jìn)行。利用該方法,唐葉峰課題組完成了7種取代類型、超過90個(gè)α-亞甲基-g-丁內(nèi)酯的合成,包括一些天然產(chǎn)物、天然產(chǎn)物核心骨架以及生物探針分子,充分展現(xiàn)了該方法的普適性和實(shí)用性。
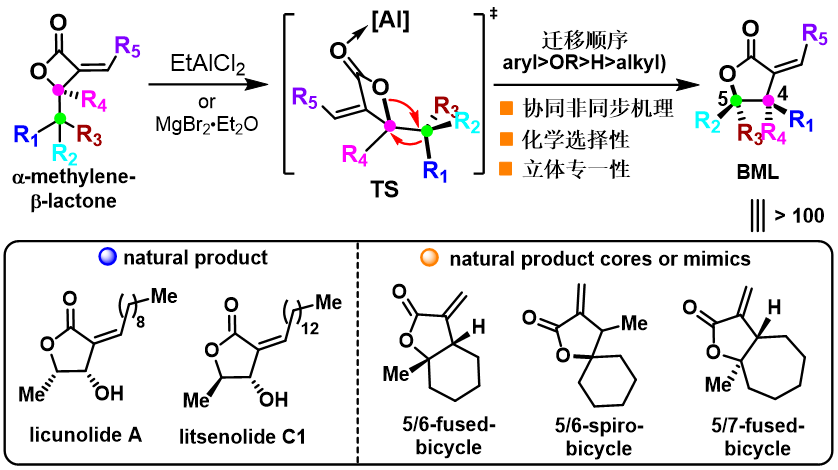
圖2. α-亞甲基-b-環(huán)丙內(nèi)酯dyotropic重排反應(yīng)研究及應(yīng)用
研究階段二:化合物的活性篩選及作用機(jī)制研究
王戈林課題組對(duì)上述合成工作中獲得的化合物進(jìn)行了活性篩選。初步結(jié)果顯示,其中一些化合物對(duì)多種腫瘤細(xì)胞具有顯著的抑制活性。進(jìn)一步研究表明,該類化合物的抗腫瘤靶點(diǎn)和作用機(jī)制較為新穎,值得進(jìn)一步深入探索,相關(guān)工作目前正在進(jìn)行當(dāng)中。
以上研究于2020年12月22日由清華大學(xué)藥學(xué)院唐葉峰課題組與王戈林課題組合作在《德國(guó)應(yīng)用化學(xué)》(Angew. Chem. Int. Ed)上發(fā)表,論文標(biāo)題為“環(huán)張力驅(qū)動(dòng)的dyotropic重排反應(yīng):一種經(jīng)由擴(kuò)環(huán)方式構(gòu)建α-亞甲基-g-丁內(nèi)酯的通用方法”(Strain-Driven Dyotropic Rearrangement: A Unified Ring-Expansion Approach to α-Methylene-g-butyrolactones),該論文被期刊編輯選為“熱點(diǎn)論文(hot paper)”
該項(xiàng)研究工作化學(xué)合成部分主要由唐葉峰課題組博士生雷小強(qiáng)完成,生物活性數(shù)據(jù)由王戈林課題組博士生齊晨完成,唐葉峰教授和王戈林教授為共同通訊作者。該研究工作得到了國(guó)家自然科學(xué)基金,國(guó)家創(chuàng)新藥物重大科技計(jì)劃和佛山-清華創(chuàng)新專項(xiàng)基金的資助。
參考資料
[1] 最新研究成果 | 活性分子合成新方法| 唐葉峰課題組和王戈林課題組合作在天然產(chǎn)物和藥物分子“優(yōu)勢(shì)骨架”合成方面取得新進(jìn)展,http://www.sps.tsinghua.edu.cn/cn/news/achievement/2021/0105/708.html
[2] 論文鏈接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202013169
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn