

近日,北京化工大學有機無機復合材料國家重點實驗室陳建峰院士、甘志華教授、中國醫學科學院昆明醫學生物學研究所和占龍教授與美國加州大學洛杉磯分校盧云峰教授等組成的國際合作研究團隊,開發了一種潛在的可用于新冠肺炎治療的方法,針對COVID-19發病過程中活性氧自由基(ROS)誘導的細胞炎癥因子風暴,利用氧化氫酶的納米膠囊n(CAT),成功調節ROS達到阻斷COVID-19病程的目的,這可能為COVID-19或者其他炎癥的治療提供一種有效的治療手段。相關研究結果近期發表于Advanced Materials期刊(DOI: 10.1002/adma.202004901)。該論文第一作者是北京化工大學秦蒙副教授,美國加州大學洛杉磯分校的曹正、溫靜博士。
根據研究發現,活性氧(ROS)水平的升高與炎癥、氧化損傷以及病毒感染和復制密切相關,因此研究人員推測調節COVID-19患者的活性氧水平可能對治療炎癥過度有效,保護組織免受氧化損傷,抑制病毒復制。如圖一所示,感染SARS-CoV-2后,白細胞被吸引到感染部位,釋放細胞因子和ROS。ROS水平升高促進病毒復制,引起氧化損傷,并通過DNA損傷、脂質過氧化和蛋白質氧化誘導細胞凋亡,血管通透性增大,進一步加劇免疫反應。結果,越來越多的白細胞被招募,進一步釋放ROS和細胞因子,導致炎癥過度和細胞因子風暴綜合征。因此阻斷ROS水平升高成為阻斷細胞因子風暴關鍵。
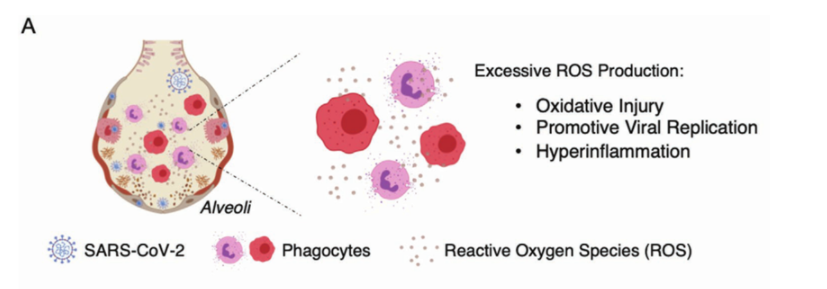
圖一. ROS引起的病理反應示意圖
ROS的產生與代謝如(圖二)所示,O2在體內代謝的過程中,產生超氧陰離子(·O2?),在超氧化物歧化酶(SOD)的介導下迅速轉化為過氧化氫(H2O2)。H2O2化學性質穩定,能夠穿過細胞膜并在組織中擴散。 H2O2的代謝主要是通過過氧化氫酶(CAT)分解成 H2O和O2。在病理條件下,ROS產生過多,但抗氧化酶缺乏,H2O2可能會局部或系統地積累,氧化含硫殘基蛋白質,并與過渡金屬(如鐵)反應,產生下游高活性的ROS。因此,消除過量的H2O2對減少下游ROS的形成至關重要,預防氧化損傷,避免免疫過激。
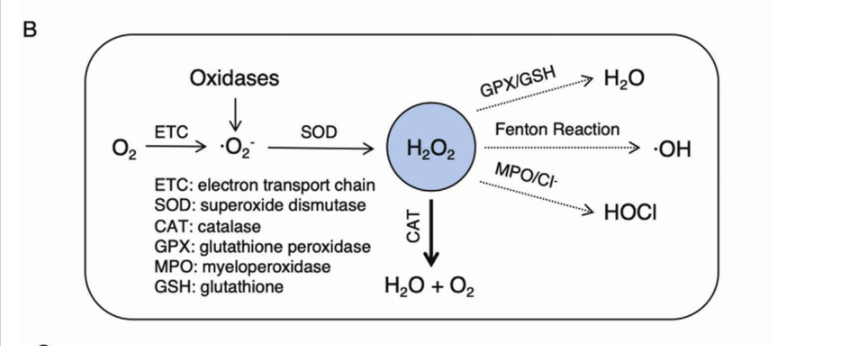
圖二. ROS的產生與代謝途徑
過氧化氫酶在體內廣泛存在于肝臟、紅細胞和肺泡上皮細胞中,是分解H2O2的最有效催化劑。一個過氧化氫酶分子可以在1s內分解107個H2O2分子。而且它是一種安全的、常用的食品添加劑和膳食補充劑,極易獲得。然而,較差的穩定性和極短的血漿半衰期(0.5h)限制了它作為藥物的應用。
為了探索其治療用途,如圖三所示,研究者利用磷脂膽堿類等單體通過非共價相互作用富集在過氧化氫酶分子周圍,與交聯劑一起聚合成一層薄薄的外殼,形成粒徑為25-30nm的納米膠囊,稱為n(CAT)。允許過氧化氫快速通過外殼與酶反應,賦予n(CAT)和天然過氧化氫酶相似的高酶活性、并顯著增強穩定性,降低免疫原性。
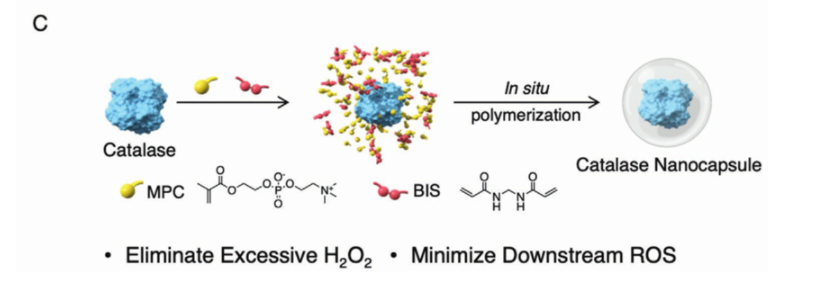
圖三:過氧化氫酶納米膠囊的設計、制備示意圖
通過與肺上皮細胞、人白細胞及H2O2共培養的一系列細胞實驗表明n(CAT)不僅具有保護細胞免受氧化損傷的能力,還可以作為免疫調節劑顯著下調人白細胞分泌的TNF-α和IL-10的量,有效阻斷炎癥反應。在小鼠的體內實驗中,霧化給藥后,n(CAT)幾乎只滯留于肺部,而在靜脈給藥后,有效到達肺及其他組織,血清半衰期為8.9h,比天然CAT(0.5h)長16.8倍。值得注意的是,通過對恒河猴進行霧化給藥,并通過鼻拭子與咽拭子取樣檢測,在確定支氣管、肺、淋巴各組織的病毒載量的基礎上進一步證實n(CAT) 能夠抑制SARS-CoV-2在恒河猴體內的復制和侵染。同時,該納米粒子不僅在人類白細胞、肺泡上皮細胞以及健康小鼠體內未見毒性,而且大劑量靜脈注射施用于恒河猴身上,通過組織切片以及血常規,肝腎功能檢測均未見任何明顯毒性。
綜上所述,過氧化氫酶具有顯著的抗炎作用和調節白細胞中細胞因子的生成的作用,保護肺泡細胞免受氧化損傷,以及抑制SARS-CoV-2在恒河猴體內的復制的能力,而沒有明顯的毒性。此外,值得注意的是,過氧化氫酶是一種安全的、常用的食品添加劑和膳食補充劑。目前,通過與北京賽升公司合作,北京化工大學已經完成n(CAT)的中試規模化制備,可以在一周內完成1萬人次使用的藥品生產,這可能為COVID-19或者其他重癥炎癥的治療提供一種有效的治療手段。
原文鏈接:https://doi.org/10.1002/adma.202004901
來源 | 北京化工大學
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn