



一、藥品注冊(cè)申請(qǐng)受理情況
2019年,藥審中心受理新注冊(cè)申請(qǐng)8082件(含器械組合產(chǎn)品5件,以受理號(hào)計(jì),下同),其中需技術(shù)審評(píng)的注冊(cè)申請(qǐng)6199件(含4907件需藥審中心技術(shù)審評(píng)和行政審批的注冊(cè)申請(qǐng)),直接行政審批(無(wú)需技術(shù)審評(píng),下同)的注冊(cè)申請(qǐng)1878件。
(一)總體情況
藥審中心受理的8077件藥品注冊(cè)申請(qǐng)中,化學(xué)藥注冊(cè)申請(qǐng)受理量為6475件,占2019年全部注冊(cè)申請(qǐng)受理量的80.2%,2016-2019年各類藥品注冊(cè)申請(qǐng)受理情況詳見圖1。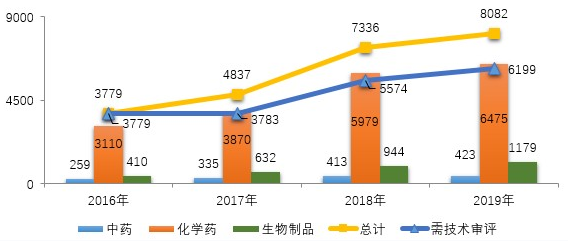
圖1 2016-2019年各類藥品注冊(cè)申請(qǐng)受理情況
藥審中心受理1類創(chuàng)新藥注冊(cè)申請(qǐng)共700件(319個(gè)品種),(化學(xué)藥的品種數(shù)以活性成分統(tǒng)計(jì),中藥和生物制品的品種數(shù)均以藥品通用名稱統(tǒng)計(jì),下同),品種數(shù)較2018年增長(zhǎng)了20.8%。其中,受理1類創(chuàng)新藥的新藥臨床試驗(yàn)(IND)申請(qǐng)302個(gè)品種,較2018年增長(zhǎng)了26.4%;受理1類創(chuàng)新藥的新藥上市申請(qǐng)(NDA)17個(gè)品種,較2018年減少了8個(gè)品種。
(二)國(guó)產(chǎn)創(chuàng)新藥受理情況
藥審中心受理國(guó)產(chǎn)1類創(chuàng)新藥注冊(cè)申請(qǐng)528件(244個(gè)品種),其中受理臨床申請(qǐng)503件(228個(gè)品種),上市申請(qǐng)25件(16個(gè)品種)。按藥品類型統(tǒng)計(jì),化學(xué)藥401件(144個(gè)品種),生物制品127件(100個(gè)品種),創(chuàng)新藥的適應(yīng)癥主要集中在抗腫瘤、抗感染和消化系統(tǒng)疾病領(lǐng)域。
(三)進(jìn)口創(chuàng)新藥及原研藥受理情況
藥審中心受理5.1類化學(xué)藥進(jìn)口原研藥注冊(cè)申請(qǐng)157件(92個(gè)品種),受理1類進(jìn)口創(chuàng)新藥注冊(cè)申請(qǐng)172件(75個(gè)品種),創(chuàng)新藥的適應(yīng)癥主要集中在抗腫瘤、內(nèi)分泌和神經(jīng)系統(tǒng)疾病領(lǐng)域。
(四)各類注冊(cè)申請(qǐng)受理情況
1.化學(xué)藥注冊(cè)申請(qǐng)受理情況
藥審中心受理化學(xué)藥注冊(cè)申請(qǐng)6475件,其中受理化學(xué)藥IND申請(qǐng)694件,較2018年增長(zhǎng)了51.9%;受理化學(xué)藥NDA 130件,較2018年增長(zhǎng)了21.5%;受理仿制藥上市申請(qǐng)(ANDA)1047件,較2018年增長(zhǎng)了6.6%;受理一致性評(píng)價(jià)補(bǔ)充申請(qǐng)1038件(308個(gè)品種),件數(shù)較2018年增長(zhǎng)71%。2019年化學(xué)藥各類注冊(cè)申請(qǐng)受理情況詳見圖3。2016-2019年化學(xué)藥IND申請(qǐng)、NDA和一致性評(píng)價(jià)等注冊(cè)申請(qǐng)受理情況詳見圖4。
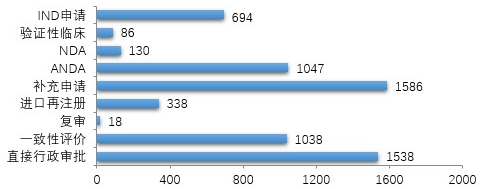
圖3 2019年化學(xué)藥各類注冊(cè)申請(qǐng)受理情況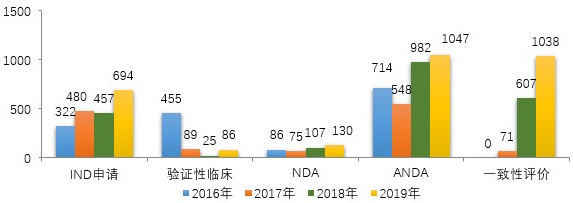
圖4 2016-2019年化學(xué)藥IND申請(qǐng)、NDA和一致性評(píng)價(jià)等
注冊(cè)申請(qǐng)受理情況
注:藥審中心自2017年8月開始承擔(dān)仿制藥質(zhì)量和療效一致性評(píng)價(jià)工作
(1)國(guó)產(chǎn)、進(jìn)口化學(xué)藥IND申請(qǐng)、NDA受理情況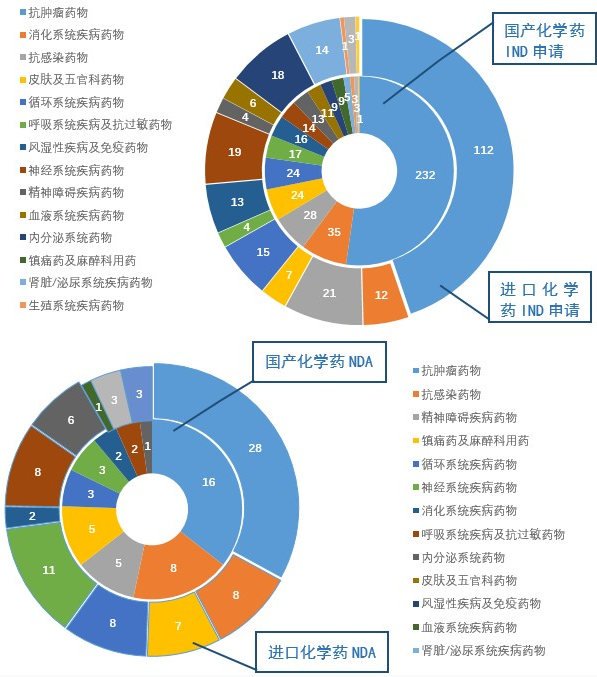
圖5 2019年受理國(guó)產(chǎn)和進(jìn)口的化學(xué)藥IND申請(qǐng)、NDA治療領(lǐng)域分布情況
在化學(xué)藥IND申請(qǐng)中,受理國(guó)產(chǎn)化學(xué)藥IND申請(qǐng)444件,受理進(jìn)口IND申請(qǐng)250件。國(guó)產(chǎn)化學(xué)藥IND申請(qǐng)的適應(yīng)癥主要集中在抗腫瘤、消化系統(tǒng)和抗感染藥物領(lǐng)域,進(jìn)口IND申請(qǐng)的適應(yīng)癥主要集中在抗腫瘤、抗感染藥物和神經(jīng)系統(tǒng)領(lǐng)域。
化學(xué)藥NDA中,受理國(guó)產(chǎn)化學(xué)藥NDA 45件,受理進(jìn)口化學(xué)藥NDA 85件。國(guó)產(chǎn)化學(xué)藥NDA的適應(yīng)癥主要集中在抗腫瘤和抗感染藥物領(lǐng)域,進(jìn)口化學(xué)藥NDA的適應(yīng)癥主要集中在抗腫瘤和神經(jīng)系統(tǒng)領(lǐng)域。2019年受理國(guó)產(chǎn)和進(jìn)口的化學(xué)藥IND申請(qǐng)、NDA治療領(lǐng)域分布情況詳見圖5。
(2)1類化學(xué)藥創(chuàng)新藥受理情況
藥審中心受理1類化學(xué)藥創(chuàng)新藥注冊(cè)申請(qǐng)573件(219個(gè)品種),品種數(shù)較2018年增加了39.5%,其中受理IND申請(qǐng)206個(gè)品種,較2018年增長(zhǎng)了46.1%;受理NDA 13個(gè)品種,較2018年減少了3個(gè)。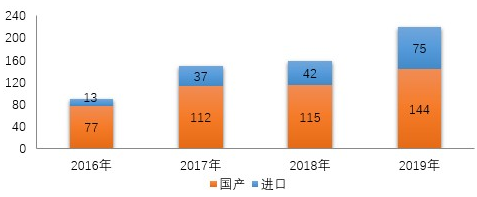
圖6 2016-2019年化學(xué)藥創(chuàng)新藥注冊(cè)申請(qǐng)受理情況
219個(gè)品種的1類化學(xué)藥創(chuàng)新藥注冊(cè)申請(qǐng)中,國(guó)產(chǎn)化學(xué)藥創(chuàng)新藥注冊(cè)申請(qǐng)為144個(gè)品種,進(jìn)口化學(xué)藥創(chuàng)新藥注冊(cè)申請(qǐng)為75個(gè)品種。2016-2019年創(chuàng)新藥注冊(cè)申請(qǐng)受理情況詳見圖6。
3.生物制品注冊(cè)申請(qǐng)受理情況
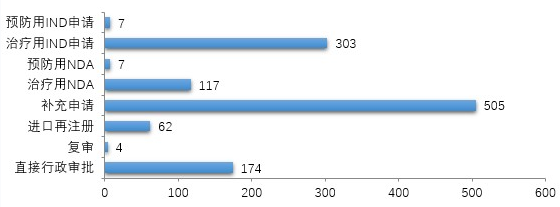
圖9 2019年生物制品各類注冊(cè)申請(qǐng)受理情況
藥審中心受理生物制品注冊(cè)申請(qǐng)1179件,其中受理生物制品IND申請(qǐng)310件(預(yù)防用IND申請(qǐng)7件,治療用IND申請(qǐng)303件),較2018年增長(zhǎng)了4%;受理生物制品NDA 124件(預(yù)防用NDA 7件,治療用NDA 117件),較2018年增長(zhǎng)了45.9%。2019年生物制品各類注冊(cè)申請(qǐng)受理情況詳見圖9。2016-2019年生物制品IND申請(qǐng)和NDA受理情況詳見圖10。
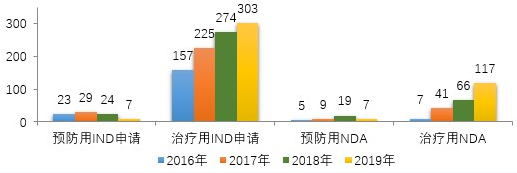
圖10 2016-2019年生物制品IND申請(qǐng)和NDA受理情況
(1)I類生物制品創(chuàng)新藥受理情況
藥審中心受理1類生物制品創(chuàng)新藥注冊(cè)申請(qǐng)127件(100個(gè)品種),件數(shù)較2018年增長(zhǎng)了3.3%,其中預(yù)防用生物制品2件,治療用生物制品125件。1類生物制品創(chuàng)新藥注冊(cè)申請(qǐng)中,IND申請(qǐng)121件(96個(gè)品種),較2018年增長(zhǎng)了8%;NDA 6件(4個(gè)品種,均為治療用生物制品),較2018年減少了5件。
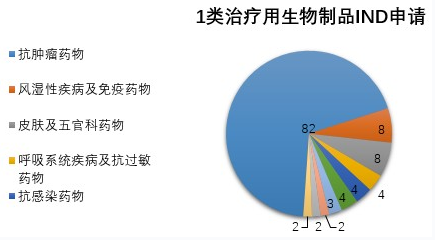
圖11 2019年受理的1類治療用生物制品IND申請(qǐng)治療領(lǐng)域分布情況
藥審中心受理1類治療用生物制品IND申請(qǐng)119件(95個(gè)品種),適應(yīng)癥主要集中在抗腫瘤治療領(lǐng)域,占全部1類治療用生物制品IND申請(qǐng)的69%,具體治療領(lǐng)域分布詳見圖11。
二、藥品注冊(cè)申請(qǐng)審評(píng)審批情況
(一)總體完成情況
1.全年審評(píng)審批完成情況
2015年至2018年期間藥審中心通過(guò)擴(kuò)充審評(píng)通道、強(qiáng)化審評(píng)項(xiàng)目管理、大規(guī)模招聘人員、借調(diào)省局人員等措施多渠道擴(kuò)增審評(píng)力量、提高審評(píng)效率,使得藥品注冊(cè)申請(qǐng)積壓基本得以解決,藥審中心的工作重點(diǎn)已經(jīng)由解決藥品注冊(cè)申請(qǐng)積壓逐漸過(guò)渡為提升藥品注冊(cè)申請(qǐng)的按時(shí)限審評(píng)審批率,2019年藥審中心實(shí)現(xiàn)了中藥、化學(xué)藥、生物制品各類注冊(cè)申請(qǐng)按時(shí)限審評(píng)審批率超過(guò)90%,基本完成了國(guó)務(wù)院《關(guān)于改革藥品醫(yī)療器械審評(píng)審批制度的意見》(國(guó)發(fā)〔2015〕44號(hào),以下簡(jiǎn)稱44號(hào)文件)確定2018年實(shí)現(xiàn)按規(guī)定時(shí)限審批的工作目標(biāo)。
2019年完成審評(píng)審批的注冊(cè)申請(qǐng)共8730件(含器械組合產(chǎn)品5件),其中完成需技術(shù)審評(píng)的注冊(cè)申請(qǐng)6817件(含4075件需藥審中心技術(shù)審評(píng)和行政審批注冊(cè)申請(qǐng)),完成直接行政審批的注冊(cè)申請(qǐng)1908件。2019年底在審評(píng)審批和等待審評(píng)審批的注冊(cè)申請(qǐng)已由2015年9月高峰時(shí)的近22000件降至4423件(不含完成審評(píng)因申報(bào)資料缺陷等待申請(qǐng)人回復(fù)補(bǔ)充資料的注冊(cè)申請(qǐng)),鞏固了44號(hào)文件要求解決注冊(cè)申請(qǐng)積壓的改革成效。
2019年4423件在審評(píng)審批和等待審評(píng)審批的注冊(cè)申請(qǐng)中,啟動(dòng)審評(píng)3334件,審評(píng)結(jié)束等待核查450件,處于暫停審評(píng)計(jì)時(shí)等待關(guān)聯(lián)品種(290件)、等待申請(qǐng)人核對(duì)質(zhì)標(biāo)說(shuō)明書包裝標(biāo)簽工藝(235件)、等待檢驗(yàn)報(bào)告(36件)等情況中的任務(wù)共639件。
完成技術(shù)審評(píng)的6817件注冊(cè)申請(qǐng)中,中藥注冊(cè)申請(qǐng)300件,生物制品注冊(cè)申請(qǐng)1104件,化學(xué)藥注冊(cè)申請(qǐng)為5413件,化學(xué)藥注冊(cè)申請(qǐng)約占全部審評(píng)完成量的79%。
2.各類注冊(cè)申請(qǐng)審評(píng)完成情況
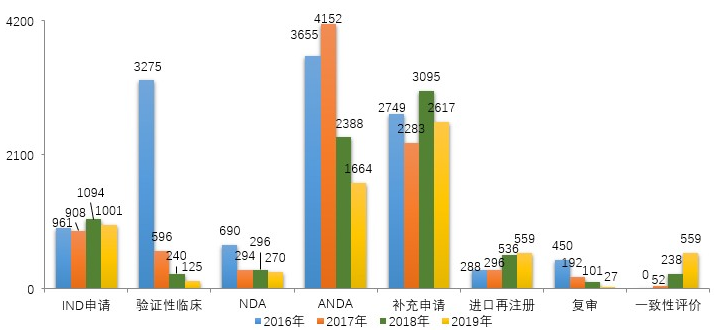
圖12 2016-2019年各類注冊(cè)申請(qǐng)審評(píng)完成情況
注:2019年含5件器械組合產(chǎn)品的注冊(cè)申請(qǐng),故上圖中2019年注冊(cè)申請(qǐng)總量大于中藥、化學(xué)藥、生物制品注冊(cè)申請(qǐng)之和。
藥審中心完成IND申請(qǐng)審評(píng)1001件(含1件器械組合產(chǎn)品),完成NDA審評(píng)270件(含1件器械組合產(chǎn)品),完成ANDA審評(píng)1664件(含3件藥械組合產(chǎn)品)。2016-2019年各類注冊(cè)申請(qǐng)審評(píng)完成情況詳見圖12。
3.審評(píng)通過(guò)情況
2019年,藥審中心審評(píng)通過(guò)批準(zhǔn)IND申請(qǐng)926件,審評(píng)通過(guò)NDA 164件,審評(píng)通過(guò)ANDA 654件,審評(píng)通過(guò)批準(zhǔn)口服固體制劑一致性評(píng)價(jià)申請(qǐng)260件(按活性成分統(tǒng)計(jì)95個(gè)品種,按通用名統(tǒng)計(jì)107個(gè)品種,詳見附表1),品種數(shù)較2018年(57個(gè)品種)同比增長(zhǎng)66.7%。
審評(píng)通過(guò)上市1類創(chuàng)新藥10個(gè)品種,審評(píng)通過(guò)進(jìn)口原研藥58個(gè)品種(含新適應(yīng)癥),具體品種詳見附表2、3。
(二)化學(xué)藥注冊(cè)申請(qǐng)審評(píng)完成情況
1.總體情況
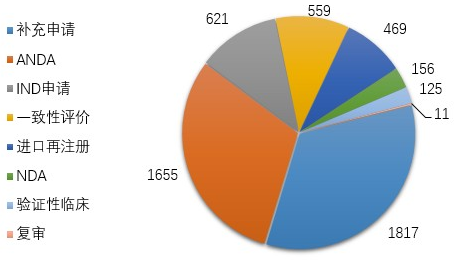
圖13 2019年化學(xué)藥各類注申請(qǐng)的審評(píng)完成情況
藥審中心完成審評(píng)的化學(xué)藥注冊(cè)申請(qǐng)5413件,其中完成化學(xué)藥臨床申請(qǐng)(IND申請(qǐng)和驗(yàn)證性臨床)共746件,完成化學(xué)藥NDA 156件,完成化學(xué)藥ANDA 1655件。2019年化學(xué)藥各類注冊(cè)申請(qǐng)的審評(píng)完成情況詳見圖13。
2.審評(píng)通過(guò)情況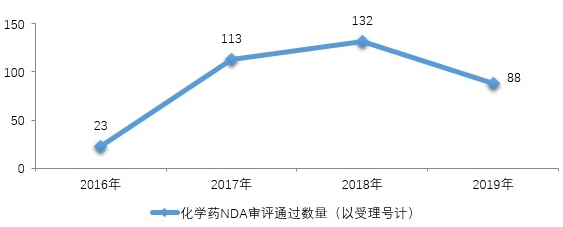
圖14 2016-2019年化學(xué)藥NDA審評(píng)通過(guò)數(shù)量情況
表1 2019年化學(xué)藥各類注冊(cè)申請(qǐng)審評(píng)完成的具體情況
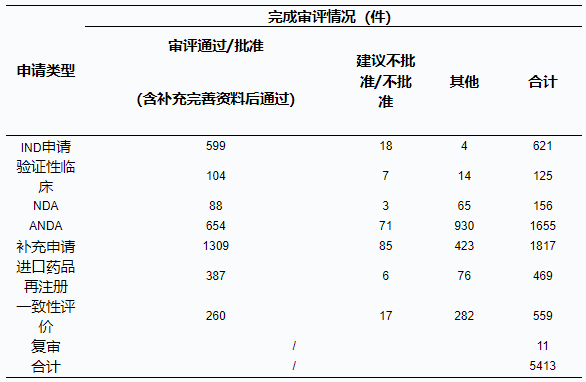
注:“其他”是指申請(qǐng)人主動(dòng)申請(qǐng)撤回的注冊(cè)申請(qǐng)、完成審評(píng)等待申請(qǐng)人補(bǔ)充完善申報(bào)資料的注冊(cè)申請(qǐng)、非藥審中心審評(píng)報(bào)送國(guó)家局藥品注冊(cè)管理司的注冊(cè)申請(qǐng)、送國(guó)家局醫(yī)療器械技術(shù)審評(píng)中心的藥械組合注冊(cè)申請(qǐng)和關(guān)聯(lián)制劑撤回的原料/輔料注冊(cè)申請(qǐng)等,下同。
藥審中心完成審評(píng)的化學(xué)藥NDA共156件,其中審評(píng)通過(guò)88件。2016-2019年化學(xué)藥NDA審評(píng)通過(guò)數(shù)量情況詳見圖14,2019年化學(xué)藥各類注冊(cè)申請(qǐng)審評(píng)完成的具體情況詳見表1。
藥審中心完成審評(píng)的化學(xué)藥IND申請(qǐng)621件,審評(píng)通過(guò)批準(zhǔn)IND申請(qǐng)599件,其中批準(zhǔn)1類化學(xué)藥創(chuàng)新藥IND申請(qǐng)493件(189個(gè)品種)。2016-2019年1類化學(xué)藥創(chuàng)新藥IND申請(qǐng)審評(píng)通過(guò)批準(zhǔn)數(shù)量詳見圖15。
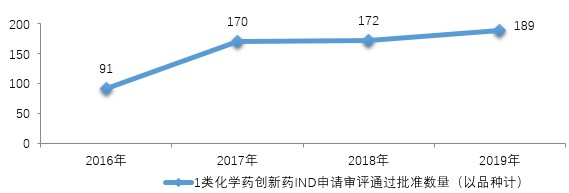
圖15 2016-2019年1類化學(xué)藥創(chuàng)新藥IND申請(qǐng)審評(píng)通過(guò)批準(zhǔn)數(shù)量
藥審中心審評(píng)通過(guò)批準(zhǔn)IND申請(qǐng)的189個(gè)1類化學(xué)藥創(chuàng)新藥中,抗腫瘤藥物、消化系統(tǒng)疾病藥物、抗感染藥物和神經(jīng)系統(tǒng)疾病藥物較多,占全部創(chuàng)新藥臨床試驗(yàn)批準(zhǔn)數(shù)量的70%。2019年審評(píng)審批IND申請(qǐng)的1類化學(xué)藥創(chuàng)新藥適應(yīng)癥分布詳見圖16。
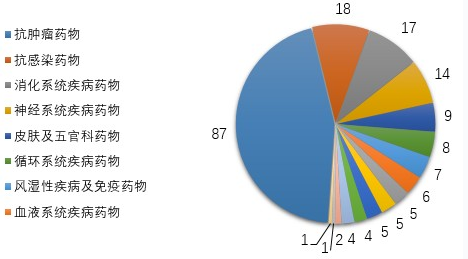
圖16 2019年審評(píng)審批IND申請(qǐng)的1類化學(xué)藥創(chuàng)新藥適應(yīng)癥分布
注:部分化學(xué)藥創(chuàng)新藥有多個(gè)適應(yīng)癥分布在不同的適應(yīng)癥分組中,故上圖中各適應(yīng)癥分組創(chuàng)新藥品種數(shù)之和大于189個(gè)。
聲明:化學(xué)加刊發(fā)或者轉(zhuǎn)載此文只是出于傳遞、分享更多信息之目的,并不意味認(rèn)同其觀點(diǎn)或證實(shí)其描述。若有來(lái)源標(biāo)注錯(cuò)誤或侵犯了您的合法權(quán)益,請(qǐng)作者持權(quán)屬證明與本網(wǎng)聯(lián)系,我們將及時(shí)更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn