

制備手性分子的一對對映異構體是不對稱合成的基本任務,其對于藥物化學和材料科學具有重要意義。在一般的不對稱合成反應中可以通過改變手性源(如手性底物、輔基、試劑、催化劑/配體等)的絕對構型來獲取產物的不同對映異構體(圖1a)。然而自然界中一些手性源分子僅以單一對映異構體的形式存在,因此難以通過這類手性源分子主導調控的不對稱合成反應制備不同絕對構型的目標產物。
另一方面,反應時長也是可以用來調控不對稱合成反應產出的重要宏觀變量。動力學拆分反應就是利用了外消旋底物分子中的一對對映異構體與手性催化劑之間反應速率的差別,通過精準控制反應時長實現目標產物和底物分子單一對映異構體的富集。但是在一般的動力學拆分反應中產物分子的絕對構型仍然由手性催化劑的絕對構型決定。想要獲得產物分子的不同對映異構體仍需使用不同絕對構型的手性催化劑。
最近,中國科學院上海有機化學研究所金屬有機化學國家重點實驗室游書力研究員團隊在研究銥催化的不對稱烯丙基去芳構化反應時發現了一種獨特的“反應時長依賴的對映發散性合成”現象:在不改變反應體系中手性源絕對構型的條件下,僅通過調節反應時長即可高對映選擇性地分別獲得目標產物分子的一對對映異構體(Nature Chemistry, 2020, DOI: 10.1038/s41557-020-0489-1)(圖1b)。
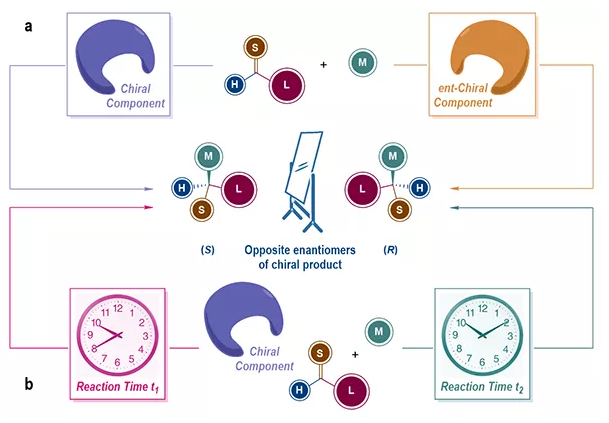
圖1 合成手性分子的一對對映異構體的策略
研究人員發現6-羥基異喹啉1a與外消旋烯丙基碳酸酯(rac)-2a在手性亞磷酰胺配體(S)-L1衍生的銥絡合物催化下可以在甲醇中發生不對稱烯丙基取代反應,生成手性烯丙基胺衍生物3aa。若控制反應時長為10小時則可以以98% ee獲得(R)構型目標產物;若將反應時長縮短至6分鐘則可以以94% ee獲得(S)構型目標產物(圖2a)。對反應體系中烯丙基胺3aa的ee值的實時監測清楚地展現出隨著反應時長的延長,目標產物的絕對構型發生反轉,并且可以在6分鐘和10小時高對映選擇性地分別獲得(S)和(R)構型的目標產物(圖2b)。也就是說,該類反應可在不改變手性催化劑絕對構型的情況下,僅通過調節反應時長,即可高對映選擇性地制備在有機合成中具有重要應用價值的手性烯丙基胺類分子的不同對映異構體。適用于該類反應的親核試劑包括一系列6-羥基異喹啉、8-羥基異喹啉和多種芳胺衍生物。
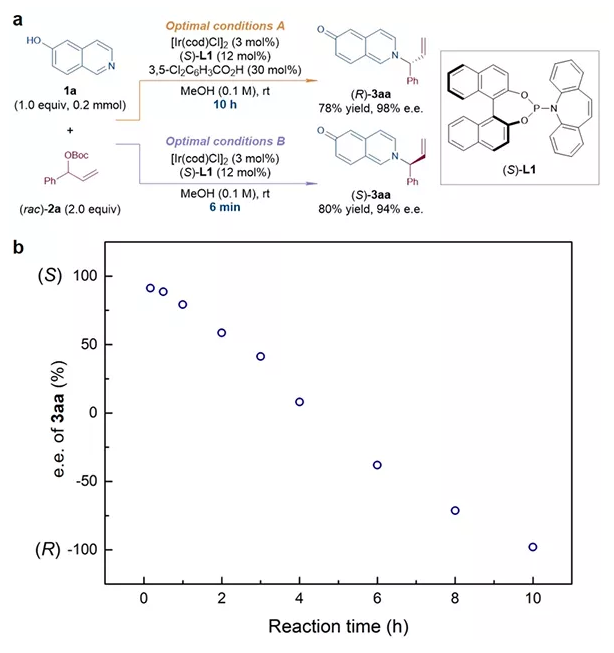
圖2 時長依賴的不對稱烯丙基取代反應
深入的機理研究表明在該反應條件下存在手性銥催化劑對烯丙基碳酸酯和烯丙基胺的兩種動力學拆分作用(圖3)。首先在(S)-L1衍生的銥催化劑存在的條件下,(S)構型烯丙基碳酸酯活性較高,可以迅速與6-羥基異喹啉反應生成(S)構型烯丙基胺(反應速率常數為k1S)。然而該產物在反應條件下并不穩定,可以在同一銥催化劑作用下與溶劑甲醇反應生成相應的烯丙基甲醚,同時釋放出6-羥基異喹啉(反應速率常數為k2S)。另一方面,活性較低的(R)構型烯丙基碳酸酯逐步與6-羥基異喹啉反應,緩慢積累(R)構型烯丙基胺(反應速率常數為k1R)。該產物在反應條件下非常穩定,不易與甲醇發生醚化反應(反應速率常數為k2R)。當兩個動力學拆分體系的反應速率彼此匹配時(k1S ? k1R ~ k2S ? k2R),即可在不同的反應時長觀察到絕對構型相反的烯丙基胺對映異構體的富集。
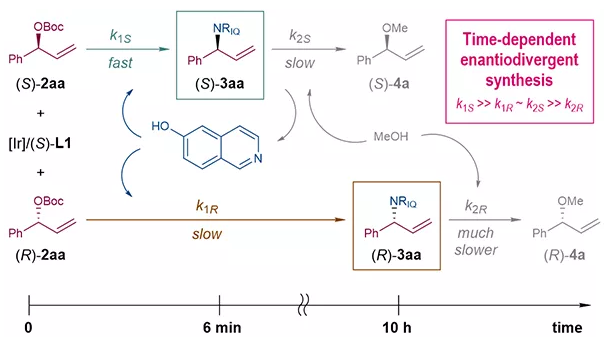
圖3 時長依賴的不對稱烯丙基取代反應的機理
“反應時長依賴的對映發散性合成”是不對稱合成中的新反應現象,其發現和反應機理研究不僅豐富了不對稱催化反應的內涵,更為手性分子不同對映體的高效制備提供了新的途徑。(文章鏈接:https://www.nature.com/articles/s41557-020-0489-1)。
上述研究工作得到了科技部、國家自然科學基金委、中國科學院、上海市科委和騰訊基金會的資助。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn