

氧化吲哚是天然產物和具有藥用價值小分子中常見的骨架之一(圖 1),因此備受化學家們的關注。
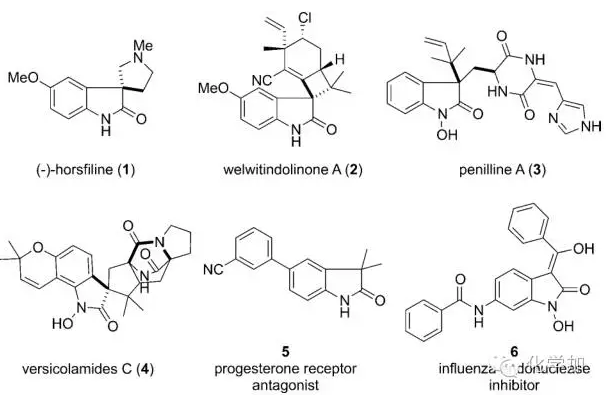
圖 1 含有氧化吲哚骨架的天然產物和藥物分子
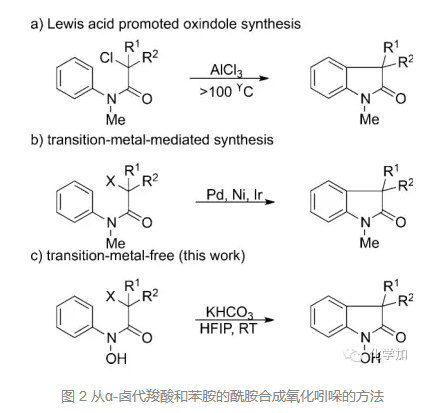
傳統的合成氧化吲哚的方法條件比較苛刻,如圖2所示:α-鹵代羧酸和苯胺的酰胺在AlCl3條件下,大于100 ℃的高溫下反應;或者需要額外的氧化劑或者比較昂貴的金屬催化劑,都不符合綠色化學的要求。因此,發展更加高效,條件更加溫和的氧化吲哚合成方法是有機化學家需要解決的一個問題。而本文就是發展了無過渡金屬、無氧化劑的合成氧化吲哚的方法。
氮雜氧化的烯丙基陽離子(Azaoxyallylic cations)是一類非常重要活性中間體,在許多環化反應和合成中都有應用。該中間體如果被苯環捕獲,就可以用來構建氧化吲哚骨架。
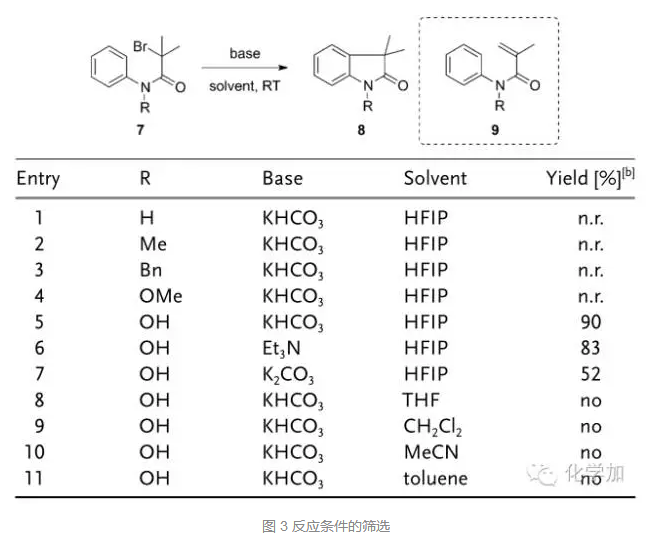
首先,作者對反應底物和條件進行了篩選,發現當酰胺氮上的取代基為OH時,KHCO3作堿,六氟異丙醇HFIP作溶劑,可以90%的高產率得到氧化吲哚骨架8,當氮上為其它取代基或者選用其它堿時,要么不反應,要么產率降低。
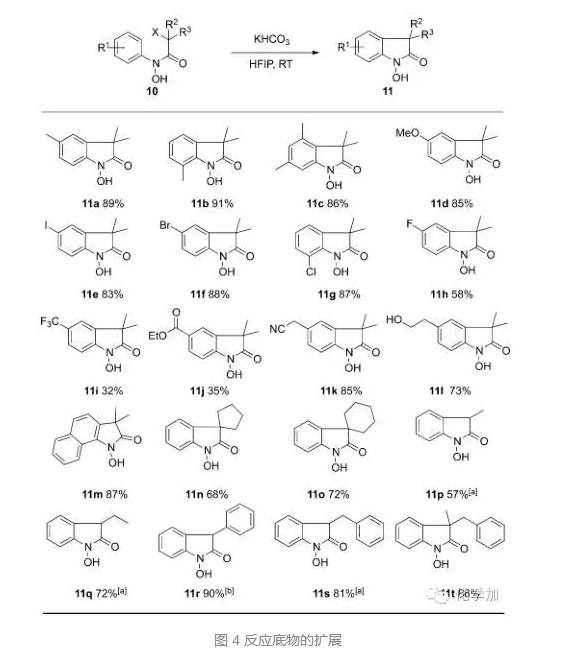
接著,作者對底物進行了擴展,當α-鹵代為溴代時,室溫反應5小時,都能取得理想的結果,苯環上取代基為鹵素、氰基、酯基、羥基等都可以兼容,當苯環上取代基為三氟甲基或者酯基時,產率降低。當α-鹵代酸α-位帶有雙烷基取代時,反應5小時,當為單取代時,需要12小時,當α-鹵代酸為氯代時,反應時間也需要延長至12小時。
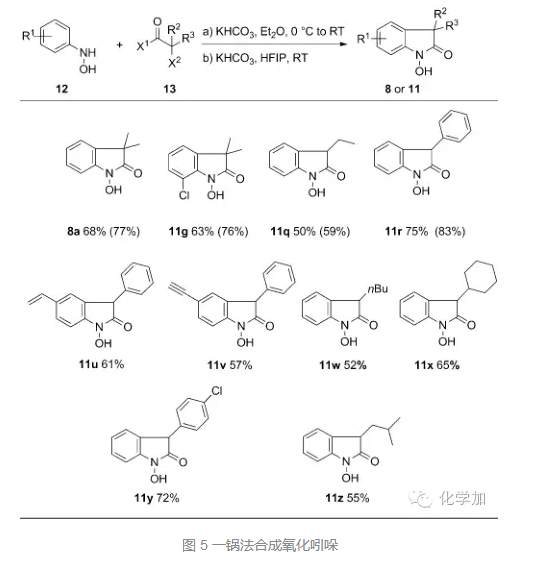
作者還嘗試了從羥基苯胺和酰氯或者酰溴出發,一鍋法先形成酰胺接著形成氧化吲哚,也取得了優秀的結果。先把底物和堿混合在乙醚中反應,旋蒸掉乙醚,不用處理接著加入KHCO3和HFIP,再反應5小時,就可以一鍋法高效合成氧化吲哚。操作簡便,產率優良,非常高效。
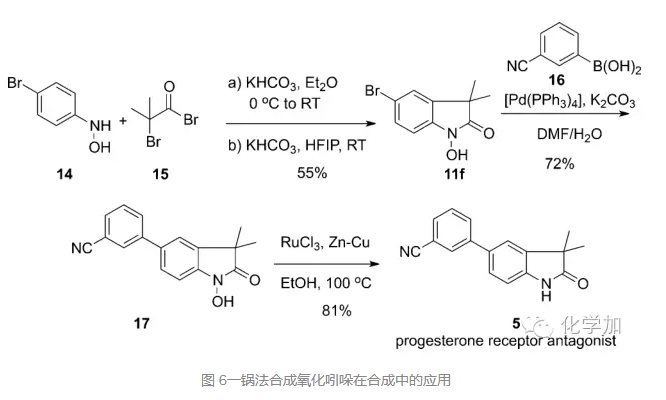
接著,作者也把該方法用于了孕激素受體拮抗劑的合成中,從羥基苯胺14和溴代酰溴15出發,一鍋法合成氧化吲哚11f,接著和芳基硼酸化合物16發生Suzuki偶聯反應得到化合物17,除去氮上羥基保護基,就可以高效地完成目標分子5。
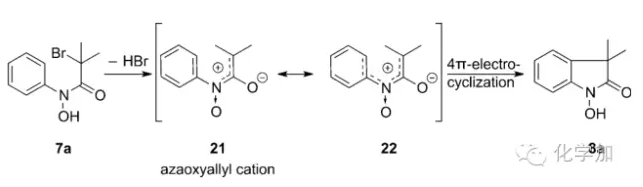
作者也根據實驗結果提出了反應可能的機理:苯胺的酰胺底物7a失去溴化氫后形成氮雜氧化烯丙基陽離子中間體21,電子離域形成更穩定的中間體22,4Π電環化關環得到目標產物8a。中間體22的形成也就可以說明為什么苯環上帶有給電子基比吸電子基如三氟甲基、酯基的底物產率高了,而六氟異丙醇溶劑則可以和22中的氧負形成氫鍵有利于反應的進行。
總結
廖學斌課題組報道了僅僅利用廉價的碳酸氫鉀作堿,六氟異丙醇作溶劑,在室溫下高效合成氧化吲哚結構的反應,由于碳酸氫鉀的堿性非常弱,官能團兼容性非常高。同時,該反應底物廉價易得,還可以通過一鍋法實現,他們也將該方法應用到孕激素受體拮抗劑的合成中。由于該反應條件溫和,操作簡單,在制藥工業中將會有廣泛的應用前景。
聲明:化學加刊發或者轉載此文只是出于傳遞、分享更多信息之目的,并不意味認同其觀點或證實其描述。若有來源標注錯誤或侵犯了您的合法權益,請作者持權屬證明與本網聯系,我們將及時更正、刪除,謝謝。 電話:18676881059,郵箱:gongjian@huaxuejia.cn